
【题目】根据以下转化关系,完成以下各空:
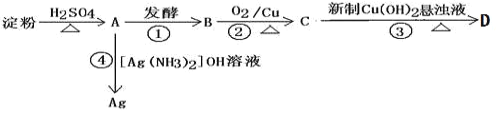
(1) A和C的结构简式:A__________________C________________。
(2) 写出②③的化学方程式:
②_______________________________________________________
③________________________________________________________
(3)④的反应类型_____________
(4)C2H518OH与D酸化后的产物反应的化学方程式______________________。
(5)用饱和碳酸钠溶液收集乙酸乙酯后,分离得到乙酸乙酯的方法是__________,分离需要的玻璃仪器有________________。
【答案】CH2OH(CHOH)4CHO CH3CHO 2CH3CH2OH + O2![]() 2CH3CHO + 2H2O CH3CHO + 2Cu(OH)2+NaOH
2CH3CHO + 2H2O CH3CHO + 2Cu(OH)2+NaOH![]() CH3COONa + Cu2O
CH3COONa + Cu2O![]() + 3H2O 氧化反应 CH3COOH+CH3CH218OH
+ 3H2O 氧化反应 CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O 分液 分液漏斗,烧杯
CH3CO18OCH2CH3+H2O 分液 分液漏斗,烧杯
【解析】
由流程图知:在稀硫酸和加热条件下,淀粉水解最终产物为葡萄糖,故A为葡萄糖,葡萄糖发酵得乙醇,故B为乙醇,乙醇催化氧化得乙醛,故C为乙醛,乙醛和新制氢氧化铜悬浊液共热得乙酸钠,则D为乙酸钠,据此填空;
(1) 按分析A为葡萄糖,结构简式为 HOCH2 (CHOH)4CHO;C为乙醛,结构简式为CH3CHO;
答案为:HOCH2 (CHOH)4CHO;CH3CHO;
(2)反应②为乙醇的催化氧化,生成乙醛和水,化学方程式为2CH3CH2OH + O2![]() 2CH3CHO + 2H2O;③为乙醛和新制的氢氧化铜悬浊液的反应,生成乙酸钠、氧化亚铜和水,化学方程式为:CH3CHO + 2Cu(OH)2+NaOH
2CH3CHO + 2H2O;③为乙醛和新制的氢氧化铜悬浊液的反应,生成乙酸钠、氧化亚铜和水,化学方程式为:CH3CHO + 2Cu(OH)2+NaOH![]() CH3COONa + Cu2O
CH3COONa + Cu2O![]() + 3H2O;
+ 3H2O;
答案为:2CH3CH2OH + O2![]() 2CH3CHO + 2H2O;CH3CHO + 2Cu(OH)2+NaOH
2CH3CHO + 2H2O;CH3CHO + 2Cu(OH)2+NaOH![]() CH3COONa + Cu2O
CH3COONa + Cu2O![]() + 3H2O;
+ 3H2O;
(3)反应④为葡糖糖和银氨溶液的反应,葡萄糖被氧化;
答案为:氧化反应;
(4) C2H518OH与D酸化后的产物反应,其中D酸化后的产物为乙酸,故为乙酸和乙醇之间的酯化反应,化学方程式为CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
答案为:CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
(5)用饱和碳酸钠溶液收集乙酸乙酯后,得到互不相溶的两层液体,故分离得到乙酸乙酯的方法是分液,需要的玻璃仪器有分液漏斗,烧杯;
答案为:分液;分液漏斗,烧杯。


科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________。
A.纯铁硬度比生铁高
B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素
D.铁在一定条件下可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为____________,形成该分散系的微粒直径范围是_________。
(3)电子工业需用30%FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式_________。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气、②铁粉、③浓硝酸、④浓盐酸、⑤烧碱、⑥浓氨水,需用用到的一组试剂是__________。
A. ①②④ B. ①③④⑥ C. ②④⑤ D. ①④⑥
(4)高铁酸钠Na2FeO3是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3X+5H2O,则X的化学式为__________。
②高铁酸钠在水中可以发生如下反应:FeO42-+10H2O=4Fe(OH)3+8OH-+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有_____性,而能够除去水中悬浮物是因为________。
③下列物质能作净水削的有_________。
a.KAl(SO4)2·12H2O b.聚合硫酸铁[Fe(OH)(SO4)]n c.ClO2 d.“84消毒液”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年诺贝尔化学奖在10月3日揭晓,弗朗西斯阿诺德、乔治史密斯和格雷戈里温特尔共同获奖,以表彰他们在酶的定向演化以及用于多肽和抗体的噬菌体展示技术方面取得的成果。如图所示是木瓜蛋白酶(蛋白质)的结构简式,下列说法不正确的是( )
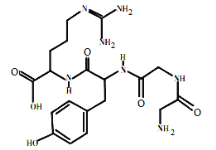
A. 醋酸铅可使木瓜蛋白酶变性
B. 木瓜蛋白酶含有苯环,属于芳香烃
C. 木瓜蛋白酶能发生水解反应、加成反应
D. 木瓜蛋白酶能与碳酸钠反应生成CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2(g)+I2(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g) H2(g)+CO(g),气体的总物质的量不再改变不能说明反应已达平衡
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1;在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2,Q2等于Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在 2 L 恒容密闭容器中 3 种物质间进行反应,X、Y、Z 的物质的量随时间的变化曲线如图所示,反应在 t1 min 时达到平衡。
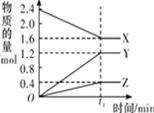
(1)请写出该反应的化学方程式:____________________________
(2)若上述反应中X、Y、Z 分别为NH3、H2、N2的一种,在此t1 min 时间内,用H2 表示该反应的平均速率υ(H2)为____________________________
(3)拆开 1mol 共价键所需吸收的能量如下表:
共价键 | H-H | N≡N | N-H |
吸收的能量/kJ | 436 | 946 | 391 |
1mol N2 完全反应生成NH3__________(填:吸收或放出多少)kJ 能量。但事实上,将 1molN2 和3molH2放在反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是________________________________
(4)下列叙述能判断该反应达到平衡状态的是___________(填字母代号)。
A.容器内各气体组分的质量分数不再发生改变
B.容器内气体的压强不再发生改变
C.容器内气体的密度不再发生改变
D.混合气体的平均相对分子质量不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。
(1)写出以下元素的名称:B________________;C______________。
(2)写出D元素在周期表中的位置___________________________
(3)用电子式表示C2D的形成过程:_______________________________
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式_______;属于_______(填“离子”或“共价”)化合物,存在的化学键的种类有______________________;写出它与水反应的离子方程式_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是物质间发生化学反应的颜色变化,其中物质a、b、c、d对应的物质正确的是( )
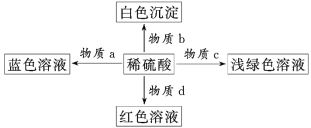
选项 | 物质a | 物质b | 物质c | 物质d |
A | Cu2(OH)2CO3 | Ba(OH)2 | Fe(OH)3 | 酚酞溶液 |
B | CuO | NaAlO2 | Fe2O3 | 紫色石蕊溶液 |
C | CuO | BaCl2 | FeO | 酚酞溶液 |
D | Cu(OH)2 | Ba(NO3)2 | FeO | 紫色石蕊溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H8的两种同分异构体X和Y。X是一种芳香烃,分子中只有一个环;Y俗称立方烷,其核磁共振氢谱显示只有一个吸收峰。下列有关说法错误的是( )
A. X、Y均能燃烧,都有大量浓烟产生
B. X既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,还能发生加聚反应
C. Y属于不饱和烃
D. Y的二氯代物有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量液态双氧水反应,生成氮气和水蒸气,放出256.652kJ的热量。
⑴写出过氧化氢的电子式________。
⑵反应的热化学方程式为_________。
⑶此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个优点是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com