
甲、乙、丙、丁由H+、Na+、Al3+、Ba2+、OH-、Cl-、HCO 中的两种组成,可以发生如图转化,下列说法正确的是( )
中的两种组成,可以发生如图转化,下列说法正确的是( )
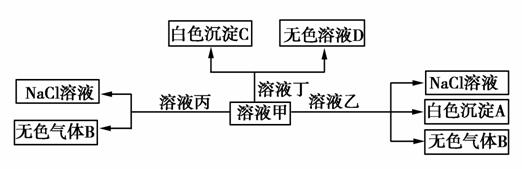
A.甲为AlCl3,乙为NaHCO3
B.溶液丙中还可以大量共存的离子有Fe2+、NO 、SO
、SO
C.在甲中滴加丁开始反应的离子方程式:HCO +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
D.白色沉淀A可能溶解在溶液D中
科目:高中化学 来源: 题型:
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
A.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点
B.原子半径:Z>Y>X
C.CaY2与水发生氧化还原反应时,CaY2只作氧化剂
D.CaY2和CaZ22种化合物中,阳离子与阴离子个数比均为1︰2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性。
B.将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO ==Fe3++NO↑+2H2O
==Fe3++NO↑+2H2O
C.HF、Al(OH)3、氨水都是弱电解质
D.蛋白质与硝酸的颜色反应、酸碱指示剂的变色反应均属化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,某水溶液中存在的离子有:Na+、B2-、HB-、H+、OH-,存在的分子有H2O、H2B。根据题意回答下列问题:
(1)写出酸H2B的电离方程式 ﹑ 。
(2)常温下,已知0.1 mol·L-1二元酸H2B溶液中c(OH-) / c(H+)=1×10-6。
①常温下,0.1 mol·L-1H2B溶液的pH= ;
②写出该酸(H2B)与少量NaOH溶液反应的离子方程式: ;
(3)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw= 。该温度下(t℃),0.1 mol·L-1HCl溶液的pH= ;
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.测定酸碱滴定曲线实验所用玻璃仪器有酸式滴定管、碱式滴定管、锥形瓶、烧杯
B.除去乙酸乙酯中混有的乙酸采用加入饱和NaOH溶液后进行分液的方法
C.除去粗盐中不溶性杂质的操作有溶解、过滤、蒸发
D.石蜡油蒸气在炽热碎瓷片的作用下分解产生的气体可使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作会导致实验结果偏高的是( )
A.用天平称量20.5 g某物质,砝码和药品的位置放反,所得药品的质量
B.测定Na2CO3溶液的pH时,先将pH试纸润湿了再测定,所测得的pH
C.配制一定物质的量浓度溶液时,定容时仰视读数,所得溶液的浓度
D.酸式滴定管在盛装标准溶液前没有用标准溶液润洗,测得的待测液浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的转化在给定条件下能一步实现的是( )
①NaAlO2(aq)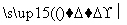 AlCl3
AlCl3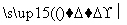 Al
Al
②NH3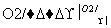 NO
NO HNO3
HNO3
③NaCl(饱和)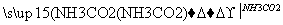 NaHCO3
NaHCO3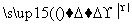 Na2CO3
Na2CO3
④FeS2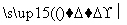 SO3
SO3 H2SO4
H2SO4
A.②③ B.①④
C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
中学化学中常见的几种物质存在如图所示的转化关系。其中,A是一种黑色粉末状固体,C是一种黄绿色气体,实验室中常用E溶液吸收多余的C。(图中部分产物和反应条件已略去)

回答下列问题:
(1)写出A与B的浓溶液反应的化学方程式:________________。
(2)固体E中含有的化学键的类型是________________,C与E溶液反应的离子方程式为________________。
(3)将B的浓溶液与H的浓溶液混合,立即产生大量气体C,该反应的离子方程式为________________。
(4)某课外小组的同学用E溶液吸收足量C后,利用如图所示装置向吸收液中持续通入SO2气体。

实验过程中观察到如下现象:
①开始时,溶液上方出现白雾,试纸a变红。甲同学认为是HCl使a变红,乙同学不同意甲的观点,乙同学认为使a变红的是_____(写出一种即可)。
②片刻后,溶液上方出现黄绿色气体,试纸b变蓝。用离子方程式解释b变蓝的原因:________________。
③最终试纸b褪色,同学们认为可能的原因有两种:一是I2有还原性,黄绿色气体等物质将其氧化成IO ,从而使蓝色消失;二是________________。
,从而使蓝色消失;二是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2的的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→ +H2O
+H2O
下列有关三聚氰胺的说法正确的是
A.分子式为C3H6N3O3 B.分子中既含极性键,又含非极性键
C.属于共价化合物 D.生成该物质的上述反应为中和反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com