
| A. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 盐酸滴在石灰石上:CO32-+2H+═CO2↑+H2O | |
| D. | 盐酸与饱和的澄清石灰水反应:H++OH-═H2O |
分析 A.铁与稀硫酸反应生成的亚铁离子;
B.碳酸钙和醋酸都不能拆开;
C.碳酸钙为难溶物,离子方程式中不能拆开;
D.澄清石灰水中的氢氧化钙需要拆开,盐酸与氢氧化钙反应生成氯化钙和水.
解答 解:A.铁与稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═H2↑+Fe2+,故A错误;
B.醋酸为弱酸,不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故C错误;
D.盐酸与饱和的澄清石灰水反应生成氯化钙和水,反应的离子方程式为:H++OH-═H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
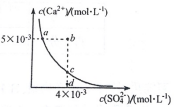 常温下,Ksp(CaSO4)=9 х 10?6,CaSO4 在水溶液中的沉淀溶解平衡曲线如图所示.下列说法不正确的是( )
常温下,Ksp(CaSO4)=9 х 10?6,CaSO4 在水溶液中的沉淀溶解平衡曲线如图所示.下列说法不正确的是( )| A. | b 点可能有沉淀生成 | |
| B. | a 点对应的Ksp 等于c 点对应的Ksp | |
| C. | 在d 点溶液中加入一定量的CaCl2可能会有沉淀析出 | |
| D. | CaSO4 溶解在水中,一定有c(Ca2+)=c(SO42-)=3×10-3mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石墨棒做电极电解氯化铜溶液,与负极相连的石墨棒上有气泡产生 | |
| B. | 氢氧燃料电池工作时氢气在负极被氧化 | |
| C. | 铅蓄电池充电时,PbSO4仅在负极生成 | |
| D. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层,这种变化属于原电池反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、H+、NO3-、Cl- | B. | H+、Na+、Cl-、CO32- | ||
| C. | Na+、Mg2+、OH-、SO42- | D. | K+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 洗净的检验是检验最后一次洗涤液中是否含有形成沉淀的该溶液中的离子 | |
| B. | 洗涤的试剂一般可选用蒸馏水、冰水、乙醇、该物质的饱和溶液 | |
| C. | 洗涤的目的一般是除去沉淀或晶体表面可溶性的杂质,提高纯度 | |
| D. | 洗涤的操作是向过滤器里加洗涤剂,一般洗涤剂尽量多加,然后让洗涤剂自然流下 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验顺序 | 实验内容 | 实验现象 | 实验顺序 | 实验内容 | 实验现象 | |
| ① | A+B | 生成白色沉淀 | ④ | B+C | 无明显变化 | |
| ② | A+C | 放出无色气体 | ⑤ | B+D | 生成白色沉淀 | |
| ③ | A+D | 放出无色气体 | ⑥ | C+D | 无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g Fe 和足量的氧气完全燃烧失去电子数为 3N A | |
| B. | 1L 浓度为 0.5mol/LFeCl3 溶液加热煮沸后,会生成 0.5molFe(OH)3胶体粒子 | |
| C. | 常温常压下,23 g NO2 和 N2O4 的混合气体一定含有 N A 个氧原子 | |
| D. | 标况下,4.48L 的水中含有 H2O 分子的数目为 0.2N A |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
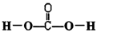 .
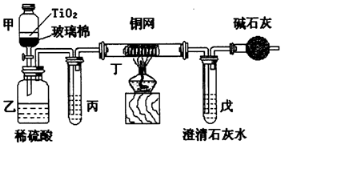
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com