
| A. | 若HA、HB均为弱酸,酸性:HA>HB,则相同条件下,溶液的pH大小为NaA>NaB | |
| B. | 相同条件下,将pH=11的NaOH溶液和和氨水分别稀释pH=9的溶液,所加水的体积前者大 | |
| C. | pH=3的醋酸与pH=1的NaOH溶液等体积混合时,溶液中离子浓度的大小顺序是:c(Na+)>c(CHCOO-)>c(OH-)>c(H+) | |
| D. | 0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2[c(HA-)+c(A2-)+c(H2A)] |
分析 A、根据酸越弱,对应的盐溶液水解程度越大分析;
B、NaOH为强碱,一水合氨为弱碱,稀释相同倍数时,强碱的pH变化大;
C、醋酸是弱酸,NaOH是强碱,氢离子浓度与氢氧根离子浓度相同时,醋酸浓度大于NaOH浓度;
D、H2A是二元弱酸,Na2A能够分步水解生成HA-和H2A,据物料守恒分析.
解答 解:A、酸越弱,对应的盐溶液水解程度越大,则若酸性HA>HB,则钠盐溶液的碱性NaA<NaB,故A错误;
B、NaOH为强碱,一水合氨为弱碱,加水稀释使其pH变化相同倍数时,一水合氨加水的体积大,故B错误;
C、pH=3的醋酸与pH=11的NaOH溶液等体积混合时溶液显酸性,所以溶液中离子浓度的大小顺序是c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;
D、在二元弱酸盐Na2A溶液中,Na2A能够分步水解生成HA-和H2A,据物料守恒可知c(Na+)═2[c(HA-)+c(A2-)+c(H2A)],故D正确;
故选D.
点评 本题考查了盐类水解、强弱电解质的区别、离子浓度大小的比较、电解质溶液中的物料守恒,题目难度中等.


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:解答题
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.
H++HA-,该滚液中由水电离出的c(H+)=10-10mol/L.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅 | B. | 硫 | C. | 铝 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸的电子式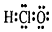 | B. | 二氧化硅的分子式:SiO2 | ||
| C. | 中子数为18的铝原子:1735Cl | D. | 钠离子的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入过量Cl2:Cl-、Fe2+、SO42-、Al3+ | |
| B. | 加入过量NaOH溶液:Na+、AlO2-、SO42-、OH- | |
| C. | 加入过量氨水:Na+、NH4+、SO42-、AlO2- | |
| D. | 加入过量铜粉:NO3-、Fe3+、SO42-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅HCl | B. | 只有HCl和HClO | C. | 只有HCl和Cl2 | D. | HCl、HClO和Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上教学质检化学试卷(解析版) 题型:选择题
1mol/L NaCl溶液表示
A.溶液里含有1mol NaCl B.1mol NaCl溶解于1L水中
C.58.5g NaCl溶于941.5g水中 D.1L水溶液中含有NaCl 58.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com