
【题目】在一定条件下,在容积为2 L的密闭容器中加入一定量的A,发生如下的反应并建立平衡:A(g)![]() 2B(g), 2B(g)
2B(g), 2B(g)![]() C(g)+2D(g)。测得平衡时各物质的浓度是:c(A)=0.3 mol·L-1,c(B)=0.2mol·L-1,c(C)=0.05mol·L-1,则最初加入的A物质的量是( )
C(g)+2D(g)。测得平衡时各物质的浓度是:c(A)=0.3 mol·L-1,c(B)=0.2mol·L-1,c(C)=0.05mol·L-1,则最初加入的A物质的量是( )
A. 0.45mol B. 0.5mol C. 0.9mol D. 1.2mol
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】人们会利用纳米级(1-100nm,1nm=10-9m)微粒物质制造出更加优秀的材料和器件,使化学在材料、能源、环境和生命科学等领域发挥越来越重要的作用。将纳米级微粒物质溶解于液体溶剂中形成一种分散系,对该分散系及分散质颗粒的叙述中正确的是( )
A. 该分散系能发生丁达尔效应 B. 该分散系为溶液
C. 该分散系属于悬浊液 D. 该分散系放置一段时间可能很快出现分层现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应A(g)+3B(g)2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是( )
A.v(A)=0.01 mol/(Ls)
B.v(B)=0.04 mol/(Ls)
C.v(B)=0.60mol/(Lmin)
D.v(C)=1.0mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4 , 发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题:
(1)反应的△H0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示.在0~60s时段,反应速率v(N2O4)为molL﹣1s﹣1反应的平衡常数K1= . 
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020molL﹣1s﹣1的平均速率降低,经10s又达到平衡.
①T100℃(填“大于”“小于”),判断理由是
②温度T时反应的平衡常数K2=
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向(填“正反应”或“逆反应”)方向移动,判断的理由是: .
(4)综合(1)、(2)小题信息你得出温度对平衡常数的影响规律是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化完全符合右图图示的是( )

①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释
④生石灰溶于水 ⑤二氧化碳与灼热的碳反应 ⑥碘的升华
⑦Ba(OH)2·8H2O与NH4Cl反应
A. ①②⑥ B. ②⑤⑦ C. ①②⑤⑥⑦ D. ②④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性。下列关于钠的叙述中,正确的是
A. 钠是银白色金属,熔点低,硬度大
B. 钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠
C. 在氧气中加热时,金属钠剧烈燃烧,发出黄色火焰
D. 金属钠着火可以用泡沫灭火器或用干燥的沙土灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置中,X,Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )
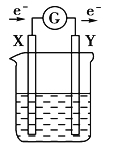
A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Zn和碳棒,则X为碳棒,Y为Zn
C. 若两电极都是金属,则它们的活动性强弱为X>Y
D. X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NH3催化还原NxOy可以消除氮氧化物的污染.
已知:反应Ⅰ:4NH3(g)+6NO(g)5N2(g)+6H2O(l)△H1
反应Ⅱ:2NO(g)+O2(g)2NO2(g)△H2 (且|△H1|=2|△H2|)
反应Ⅲ:4NH3(g)+6NO2(g)5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如表
温度/K | 反应I | 反应II | 已知: |
298 | K1 | K2 | |
398 | K1′ | K2′ |
(1)推测反应Ⅲ是反应(填“吸热”或“放热”)
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图所示.
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=
②下列说法正确的是 .
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H﹣O键与N﹣H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,分析NO2体积分数﹣﹣φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2);恒温恒容容器,φ(NO2) .
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3L,c(N2)与反应时间t变化曲线X如图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z.则:
①变为曲线Y改变的条件是 . 变为曲线Z改变的条件是
②若t2降低温度,t3达到平衡,请在图中画出曲线X在t2﹣t4内 c(N2)的变化曲线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已严重危害人类的生活。下列对应关系正确的是( )
选项 | 环境问题 | 造成环境问题的主要物质 |
A | 温室效应 | CO2 |
B | 南极臭氧层空洞 | SO2 |
C | 酸雨 | O3 |
D | 光化学烟雾 | N2 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com