
| 实验编号 | 反应物 | 加入物质 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 9mL 5% H2O2溶液 | 1mL 水 |
| ④ | 9mL 5% H2O2溶液 | 1mL 0.1mol•L-1 HCl溶液 |
| ⑤ | 9mL 5% H2O2溶液 | 1mL 0.1mol•L-1 NaOH溶液 |

| 物理量 实验序号 | V[30% H2O2]/mL | … | |
| 1 | a | … | |
| 2 | a | … |
分析 Ⅰ.(1)实验①和②的浓度不同;
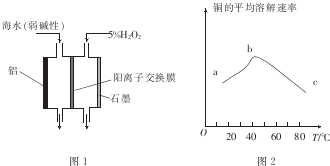
(2)由图可知,⑤的反应速率最大,④的反应速率最小,以此来解答;
Ⅱ.(3)实验时可以通过测量相同时间内产生O2的体积;
(4)探究不同浓度的Fe3+对H2O2分解的催化效果,双氧水的浓度,用量相同,催化剂的浓度不同来设计.
解答 解:Ⅰ.(1)实验①和②的浓度不同,则该实验的目的为探究浓度对化学反应速率的影响,
故答案为:浓度;
(2)由图可知,⑤的反应速率最大,④的反应速率最小,结合实验方案可知,碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率,
故答案为:碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率;
Ⅱ.(3)通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量相同时间内产生O2的体积或(产生相同体积氧气所需的时间),
故答案为:相同时间内产生O2的体积(产生相同体积氧气所需的时间);
(4)探究不同浓度的Fe3+对H2O2分解的催化效果,双氧水的浓度,用量相同,催化剂的浓度通过水体积变化来体现Fe3+浓度变化,溶液的总体积保持一致为(a+b+c)mL,设计如下表:
| 物理量 实验序号 | V[30% H2O2]/mL | V[0.1mol?L-1 Fe2(SO4)3]/mL | V[蒸馏水]/mL | t[时间]/s | V[O2]/mL |
| 1 | a | b | c | t | V1 |
| 2 | a | c | b | t | V2 |
| 物理量 实验序号 | V[30% H2O2]/mL | V[0.1mol?L-1 Fe2(SO4)3]/mL | V[蒸馏水]/mL | V[O2]/mL | t[时间]/s |
| 1 | a | b | c | V | t1 |
| 2 | a | c | b | V | t2 |
| 物理量 实验序号 | V[30% H2O2]/mL | V[0.1mol?L-1 Fe2(SO4)3]/mL | V[蒸馏水]/mL | t[时间]/s | V[O2]/mL |
| 1 | a | b | c | t | V1 |
| 2 | a | c | b | t | V2 |
| 物理量 实验序号 | V[30% H2O2]/mL | V[0.1mol?L-1 Fe2(SO4)3]/mL | V[蒸馏水]/mL | V[O2]/mL | t[时间]/s |
| 1 | a | b | c | V | t1 |
| 2 | a | c | b | V | t2 |
点评 本题考查影响化学反应速率的因素,试题能够较好的考查学生实验设计、数据处理、图象分析的综合能力,注意掌握温度、浓度、催化剂等因素对化学反应速率的影响,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| B. | 氢氧化钠溶液与稀盐酸反应:OH-+H+═H2O | |
| C. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L Na2CO3溶液:c(OH-)+c(H+)═c(HCO3-)+2c(H2CO3) | |
| B. | 0.1mol/L NH4Cl溶液:c(NH4+)+c(Cl-)═0.2mol/L | |
| C. | 向硝酸钠溶液中滴加稀盐酸得到的pH=4的混合溶液:c(Na+)═c(NO3-) | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (NH4)2Fe(SO4)2溶解于水:(NH4)2Fe(SO4)2?2NH4++Fe2++2SO42- | |
| B. | Al(OH)3在水中的电离:Al(OH)3?Al3++3OH- | |
| C. | H3PO4溶解于水:H3PO4+3H2O?3H3O++PO43- | |
| D. | NaHSO3在水中的电离:HSO3-+H3O+?SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 体积/mL 液体 | A | B | C | D |
| 0.4mol.L-1Fe2(SO4)3溶液 | 0 | 1.8 | 2.0 | V1 |
| 30%H2O2溶液 | 20.0 | 20.0 | 20.0 | 20.0 |
| HO2 | V2 | V3 | 15.0 | 13.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的水与重水含有的电子数 | |
| B. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| C. | 同温、同压、同体积的CO和NO含有的原子数 | |
| D. | 常温下等物质的量的铝分别与足量氯气、浓硝酸反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑧⑨⑩ | B. | ②④⑥⑦ | C. | ②⑤⑦⑧⑩ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2O3常用作红色油漆和涂料 | B. | 碳酸氢钠可用于治疗胃酸过多 | ||
| C. | 二氧化硅可用于制造集成电路 | D. | Cl2可用于制漂白粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com