
| A. | ①② | B. | ②③ | C. | ①④ | D. | 只有① |
分析 原子序数小于36的元素X,其原子最外层中未成对电子数最多,最外层电子数未成对电子数最多为3,则X属于第VA族元素,由此分析解答.
解答 解:原子序数小于36的元素X,其原子最外层中未成对电子数最多,最外层电子数未成对电子数最多为3,则X属于第VA族元素,在形成的阴离子中元素呈现的化合价有+3价、+5价,
①XO3-中X元素显+5价,如硝酸根离子,故①选;
②XO32-中X元素显+4价,但N、P元素不能形成酸根XO32-,故②不选;
③XO42-中的X元素显+6价,故③不选;
④P元素能形成PO43-,故④选;
故选C.
点评 本题考查原子核外电子的排布,题目难度中等,注意根据电子排布式判断未成对电子数.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3$\stackrel{电解}{→}$ Al$→_{高温}^{Fe_{2}O_{3}}$ Fe | |
| B. | S$\stackrel{O_{2}/点燃}{→}$ SO3$\stackrel{H_{2}O}{→}$ H2SO4 | |
| C. | Cu2(OH)2CO3$\stackrel{盐酸}{→}$CuCl2(aq)$\stackrel{电解}{→}$ Cu | |
| D. | Fe2O3$\stackrel{HCl(aq)}{→}$ FeCl3(aq)$\stackrel{△}{→}$ 无水FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
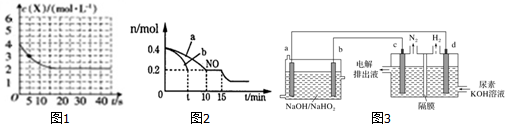
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:a<c<d<e | |
| B. | 气态氢化物的稳定性e<b<c | |
| C. | 最高价氧化物的水化物酸性b>e | |
| D. | c和d形成的化合物溶于水后溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成0.1NA根共价键 | B. | 消耗反应物总体积2.24L | ||
| C. | 转移了2NA个电子 | D. | 产物溶于水后,溶液pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 名称 | 托盘天平 (带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有2个羧基 | B. | 含有1个甲基 | ||
| C. | 含有2个羟基 | D. | 同时含有1个羟基和1个醛基 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com