
油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝的食品添加剂,逐步转换为无铝的食品添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)和碳酸氢铵(臭粉)组成。为测定试样中小苏打的质量分数ω(NaHCO3),实验小组同学设计了如下装置进行实验。

实验过程:
①按上图组装仪器,检查装置的气密性;
②将试样m1 g放入硬质玻璃管中,装置B、C、D中药品如上 图,已知加药品后装置B的质量为m2 g、装置C的质量为m3 g;
图,已知加药品后装置B的质量为m2 g、装置C的质量为m3 g;
③关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4 g、装置C的质量为m5 g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)装置B的作用为
________________________________________________________________________;
装置C的作用为
________________________________________________________________________。
(3)实验过程中通入N2的目的为
________________________________________________________________________。
(4)用下列各项所提供的数据能计算出ω(NaHCO3)的是________(填选项字母)。
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m3、m5 |
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的ω(NaHCO3),若能,写出ω(NaHCO3)的计算式。
________(填“能”或“不能”),________(若不能,此空不作答)。
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
一定温度下,某密闭容器里发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g)正反应为吸热反应,当反应达到平
CO2(g)+H2(g)正反应为吸热反应,当反应达到平 衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
①升高温度 ②增大压强 ③再通入n mol CO2和n mol H2
④再加入2n mol CO和2n mol H2O(g)
A.①② B.②④
C.③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温时,向某密闭容器中通入2 mol X和1 mol Y气体,发生如下反应 :2X(g)+Y(g)2Z(g),
:2X(g)+Y(g)2Z(g),
压强一定时,测得在平衡时Z的体积分数为0.4。
(1)与上述平衡保持同温、同压,若向密闭容器中通入4 mol X(g)和2 mol Y(g),达到平衡,则Z的体积分 数为__________;平衡时,气体的总物质的量是__________。
数为__________;平衡时,气体的总物质的量是__________。
(2)与上述平衡保持同温、同压,若向密闭容器中通入X(g)和Y(g)的物质的量分别记为n(X)、n(Y),并满足平衡时Z的体积分数为0.4,则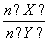 的取值范围为__________。
的取值范围为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Na2S2O3是重要的化工原料,易溶于水。在中性或碱性环境中稳定。
I.制备Na2S2O3•5H2O
反应原理:Na2SO3(aq)+S(s)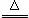 Na2S2O3(aq)
Na2S2O3(aq)
实验步骤:
①称取15g Na2SO3加入圆底烧瓶中,再加入80ml蒸馏水。另取5g研细的硫粉,用3ml 乙醇润湿,加入上述溶液中。
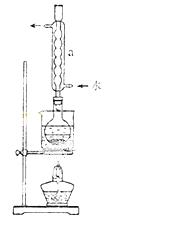
②安装实验装置(如图所示,部分加持装置略去),水浴加热,微沸60分钟。
③趁热过滤,将滤液水浴加热浓缩,冷却析出Na2S2O3•5H2O,经过滤,洗涤,干燥,得到产品。
回答问题:
(1)硫粉在反应前用乙醇润湿的目的是 。
(2)仪器a的名称是 ,其作用是 。
(3)产品中除了有未反应的Na2SO3外,最可能存在的无机杂质是 ,检验是否存在该杂质的方法是 。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子方程式表示其原因:
。
II.测定产品纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 mol•L‾1碘的标准溶液滴定。
反应原理为:2S2O32‾+I2=S4O62-+2I‾
(5)滴定至终点时,溶液颜色的变化: 。
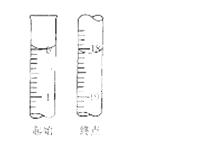
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。产品的纯度为(设Na2S2O3•5H2O相对分子质量为M) 。
III.Na2S2O3的应用
(7)Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42‾,常用作脱氧剂,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案可行的是( )
A.检验溶液中是否有SO42-时,加入BaCl2溶液,再加稀硝酸,观察沉淀是否消失
B.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
C.选用25 mL碱式滴定管量取14.80 mL 1 mol·L-1 NaOH溶液
D.检验溶液中是否含有CO32-时,加入稀盐酸,将产生的气体通入澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
已知SO2和CO2都是酸性氧化物,其化学性质具有一定的相似性;镁和钠的化学性质也有一定的相似性。氧化铜和氧化铁都是碱性氧化物,其化学性质也有一定的相似性。三个研究性学习小组分别根据不同的课题进行研究,其方案如下:

Ⅰ.第一个研究性学习小组用如图Ⅰ所示的装置进行镁粉与二氧化硫反应的实验。
(1)实验室制取二氧化硫类似于制取 二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:________。
二氧化碳,在下列物质中选择合适的试剂制取二氧化硫:________。
A.10%的硫酸 B.80%的硫酸
C.浓盐酸 D.稀硝酸
E.亚硫酸钠固体 F.亚硫酸钙固体 G.饱和亚硫酸钠溶液
(2)反应后,发现B管壁中有固体粉末产生,取反应后B管中的固体粉末溶于稀盐酸中,产生具有臭鸡蛋气味的气体,写出B管中发生反应的化学方程式:__________________________________________________。
(3)你认为该装置是否有不足之处?________。如果有,请写出改进方法: ________________________________________________________________。(如果无,此空不答)
Ⅱ.第二个研究性学习小组利用图Ⅱ所示装置来探究氨气的还原性。
(4)分别注明所用试剂:甲:________,乙:________,丙:氧化铜,丁:________。确定反应已发生的实验现象:_____________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 mol金属Al全部转化为Al(OH)3,消耗HCl a mol,NaOH b mol,则a+b的最小值为( )
A.4 B.6 C.8 D.16
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com