
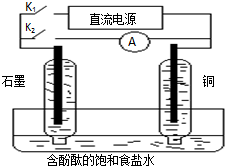
A���Ͽ�K2���պ�K1ʱ���ܷ�Ӧ�����ӷ���ʽΪ��2H++2Cl-
| ||||
| B���Ͽ�K2���պ�K1ʱ��ͭ�缫������Һ�ȱ�� | ||||
| C���Ͽ�K1���պ�K2ʱ��ͭ�缫�ϵĵ缫��ӦΪ��Cl2+2e-�T2Cl- | ||||
| D���Ͽ�K1���պ�K2ʱ��ʯī�缫������ |
| ||
| ||
| ||


 ��Ȥ������ҵ���ϿƼ�������ϵ�д�
��Ȥ������ҵ���ϿƼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��3m+2 | ||
B��3m+
| ||
C��3m+3p+
| ||
D��3m+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢۢ� | B���ڢۢ� |
| C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ܶȱ�Һ̬ˮ���ܶ�С |
| B��NH3��Һ�� |
| C������ͬ�����£�H2O�ķе��H2S�ķе�� |
| D��HF���ӱ�HCl�����ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na��O2 |
| B��NaOH��CO2 |
| C��H2��Cl2 |
| D��ľ̿��C����O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����SO2��Ӧ����Na2SO4��O2 |
| B��Na2O2Ͷ�뵽��̪��Һ�У���̪��Һ�ȱ�������ɫ |
| C��Na2O2�����ᷴӦ�����κ�ˮ������Na2O2�Ǽ��������� |
| D��Na2O2��ˮ��Ӧ��Na2O2����������ˮ�ǻ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ħ�������ʵ����ĵ�λ��ÿĦ�����ʺ���6.02��1023������ |
| B��1 mol��������Ϊ16 g |
| C��22.4L����O2Լ��1.204��1024��Oԭ�� |
| D��0.5 mol HeԼ����6.02��1023������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Դ�ǹ��÷�չ����Ҫ������
��Դ�ǹ��÷�չ����Ҫ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B����� |
| C��������� | D���Ȼ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com