
ĪŖĮĖŃŠ¾æMnO2ÓėĖ«ŃõĖ®£ØH2O2£©µÄ·“Ó¦ĖŁĀŹ£¬Ä³Ń§Éś¼ÓÉŁŠķµÄMnO2 ·ŪÄ©ÓŚ 50 mLĆܶČĪŖ1.1g?cm-3 µÄĖ«ŃõĖ®ČÜŅŗÖŠ£¬ĶعżŹµŃé²ā¶Ø£ŗŌŚ±ź×¼×“æöĻĀ·Å³öĘųĢåµÄĢå»żŗĶŹ±¼äµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£ĒėŅĄĶ¼»Ų“šĻĀĮŠĪŹĢā£ŗ
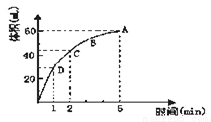
£Ø1£©ŹµŃ鏱·Å³öĘųĢåµÄ×ÜĢå»żĪŖ £»
£Ø2£©·Å³öŅ»°ėĘųĢåĖłŠčŅŖµÄŹ±¼äĪŖ £»
£Ø3£©ABCDĖĵć»Æѧ·“Ó¦ĖŁĀŹµÄÓÉæģµ½ĀżĖ³ŠņĪŖ £»
£Ø4£©ŌŚ5minŗó£¬ŹÕ¼Æµ½µÄĘųĢåĢå»ż²»ŌŁŌö¼Ó£¬ŌŅņŹĒ ”£
 ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø
ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø
Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø ¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅØĮņĖįŗĶÅØŃĪĖį³¤ĘŚ±©Ā¶ŌŚæÕĘųÖŠÅØ¶Č½µµĶ | |
| B£® | ŠĀÖĘĀČĖ®ŗĶ¹żĀČ»ÆÄʶ¼ÄÜŹ¹ŗģÄ«Ė®ĶŹÉ« | |
| C£® | ĘÆ°×·ŪŗĶĖ®²£Į§³¤ĘŚ±©Ā¶ŌŚæÕĘųÖŠ¶¼»į±äÖŹ | |
| D£® | ÅØĮņĖįŗĶÅØĻõĖį¼ÓĖ®Ļ”ŹĶŗó¶¼ÄÜÓė½šŹōĶ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģɽ¶«Ź”øßČżÉĻµŚŅ»“Ī½ĢѧÕļ¶Ļ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĄė×Ó·½³ĢŹ½ÖŠ£¬²»ÕżČ·µÄŹĒ
A£®µČĢå»żµČĪļÖŹµÄĮæÅØ¶ČµÄNaHCO3ŗĶBa£ØOH£©2Į½ČÜŅŗ»ģŗĻ£ŗ
HCO3££«Ba2£«£«OH£=BaCO3”ż£«H2O
B£®ĻņNH4Al£ØSO4£©2ČÜŅŗÖŠµĪČėBa£ØOH£©2Ē”ŗĆŹ¹SO42-ĶźČ«³Įµķ£ŗ
2Ba2+ + 4OH- + Al3+ + 2SO42- = 2BaSO4”ż+ AlO2- + 2H2O
C£®ĻņMg£ØHCO3£©2ČÜŅŗÖŠ¼ÓČė¹żĮæµÄNaOHČÜŅŗ£ŗ
Mg2+ + 2HCO-3 + 4OH- = Mg£ØOH£©2”ż+ 2CO32- + 2H2O
D£®ĻņFe£ØNO3£©2ČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖį£ŗ
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NOӟ+ 2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017Ń§ÄźÉ½¶«Ź”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
×ī½ü£¬æĘѧ¼ŅŃŠÖĘ³öŅ»ÖÖÖ½ÖŹµē³Ų£¬ÕāÖÖ”°Čķµē³Ų”±²ÉÓƱ”²ćÖ½Ę¬×÷ĪŖŌŲĢåŗĶ“«µ¼Ģ壬ŌŚŅ»±ßø½×Ŋ棬ŌŚĮķŅ»±ßø½×ŶžŃõ»ÆĆĢ”£µē³Ų×Ü·“Ó¦Ź½ĪŖZn£«2MnO2£«H2O===ZnO£«2MnOOH”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®øƵē³ŲÖŠZn ĪŖøŗ¼«£¬MnO2ĪŖÕż¼«
ĪŖøŗ¼«£¬MnO2ĪŖÕż¼«
B£®øƵē³ŲµÄÕż¼«·“Ó¦Ź½ĪŖMnO2£«e££«H2O==MnOOH£«OH£
C£®µ¼µēŹ±ĶāµēĀ·µē×ÓÓÉZnĮ÷ĻņMnO2£¬ÄŚµēĀ·µē×ÓÓÉMnO2Į÷ĻņZn
D£®µē³Ų¹¤×÷Ź±Ė®·Ö×ÓŗĶOH£¶¼ÄÜĶعż±”²ćÖ½Ę¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017Ń§ÄźÉ½¶«Ź”ø߶žÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓĆŹÆÄ«×÷µē¼«µē½ā1mol”¤L£1µÄCuSO4ČÜŅŗ£¬µ±c£ØCu2£«£©ĪŖ0.5mol”¤L£1Ź±£¬Ķ£Ö¹µē½ā£¬ĻņŹ£ÓąČÜŅŗÖŠ¼ÓČėĻĀĮŠŗĪÖÖĪļÖŹæÉŹ¹µē½āÖŹČÜŅŗ»Öø“ÖĮŌĄ“דĢ¬
A£®CuSO4 B£®CuO C£®Cu£ØOH£©2 D£®CuSO4”¤5H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĖÄÖÖXČÜŅŗ·Ö±š¼ÓČėĖÄøöŹ¢ÓŠ10 mL 2 mol/LŃĪĖįµÄÉÕ±ÖŠ£¬¾ł¼ÓĖ®Ļ”ŹĶµ½50 mL£¬¼ŁÉč»ģŗĻŗĶĻ”ŹĶŹĒĖ²¼äĶź³ÉµÄ£¬ŌņæŖŹ¼µÄĖ²¼ä·“Ó¦ĖŁĀŹ×ī“óµÄŹĒ£Ø £©
A£®20 mL 2 mol/L µÄXČÜŅŗ B£®10 mL 4 mol/L µÄXČÜŅŗ
C£®20 mL 3 mol/L µÄXČÜŅŗ D£®10 mL 2 mol/L µÄXČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ŌČČ»Æѧ·½³ĢŹ½C£Øs£©£«H2O£Øg£©===CO£Øg£©£«H2£Øg£© ¦¤H£½£«131.3 kJ”¤mol£1×ī×¼Č·µÄĄķ½āŹĒ
A£®1 molĢ¼ŗĶ1 molĖ®ÕōĘų·“Ӧɜ³É1 mol COŗĶ1 mol H2£¬Ķ¬Ź±ĪüŹÕ131.3 kJČČĮæ
B£®1 molĢ¼ŗĶ1 molĖ®·“Ӧɜ³É1 molCOŗĶ 1 mol H2 £¬Ķ¬Ź±·Å³ö131.3 kJČČĮæ
C£®¹ĢĢåĢ¼ŗĶĖ®ÕōĘū·“Ó¦ĪüŹÕ131.3 kJČČĮæ
D£®1øöĢ¼Ō×ÓŗĶ1øöĖ®·Ö×Ó·“Ó¦£¬ĪüČČ131.1 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĖÄ“ØŹ”³É¶¼ŹŠøßŅ»ÉĻ10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŌŚĮ½øöĆܱÕČŻĘ÷ÖŠ£¬·Ö±š³äÓŠÖŹĮæĻąĶ¬µÄ¼×”¢ŅŅĮ½ÖÖĘųĢ壬ČōĖüĆĒµÄĪĀ¶ČŗĶĆܶČĻąĶ¬£¬ŹŌøł¾Ż¼×”¢ŅŅµÄĦ¶ūÖŹĮæ£ØM£©¹ŲĻµ£¬ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ČōM£Ø¼×£©£¾M£ØŅŅ£©£¬ŌņĘųĢåĢå»ż£ŗ¼×£¼ŅŅ
B£®ČōM£Ø¼×£©£¼M£ØŅŅ£©£¬ŌņĘųĢåµÄŃ¹Ēæ£ŗ¼×£¾ŅŅ
C£®ČōM£Ø¼×£©£¾M£ØŅŅ£©£¬ŌņĘųĢåµÄĦ¶ūĢå»ż£ŗ¼×£¼ŅŅ
D£®ČōM£Ø¼×£©£¼M£ØŅŅ£©£¬ŌņµÄ·Ö×ÓŹż£ŗ¼×£¼ŅŅ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | sÄܼ¶µÄŌ×Ó¹ģµĄ³ŹĒņŠĪ£¬“¦ŌŚøĆ¹ģµĄÉĻµÄµē×ÓÖ»ÄÜŌŚĒņæĒÄŚŌĖ¶Æ | |
| B£® | pÄܼ¶µÄŌ×Ó¹ģµĄ³Ź·Ä“øŠĪ£¬Ėę×ÅÄܲćµÄŌö¼Ó£¬pÄܼ¶Ō×Ó¹ģµĄŅ²ŌŚŌö¶ą | |
| C£® | ijŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ1s22s2 2p63s2 3p63d54s1ŹōÓŚ¼¤·¢Ģ¬ | |
| D£® | Fe2+µÄµē×ÓÅŲ¼Ź½ĪŖ1s22s2 2p63s2 3p63d6 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com