
·ÖĪö £Ø1£©äå»ÆÄĘÓėÅØĮņĖįµĆµ½HBr£¬1-¶”“¼ÓėHBr·¢ÉśČ”“ś·“Ӧɜ³É1-ä嶔Ķ飻ÅØĮņĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉŅŌ½«äåĄė×ÓŃõ»ÆĪŖäåµ„ÖŹ£»
£Ø2£©Ēæ¼īČŻŅ׏¹1-ä嶔ĶéĖ®½ā£¬äå¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉŅŌÓĆ»¹ŌŠŌµÄNaHSO3ČÜŅŗ³żČ„£»
£Ø3£©Ģ¼ĖįĒāÄĘČÜŅŗĪŖČõ¼ī£¬æÉŅŌ³żČ„Ź£ÓąµÄĮņĖį£»
£Ø4£©ÅØĮņĖįÓėÓŠ»śĪļ²»»„ČÜ£¬²ÉÓĆ·ÖŅŗ·½·Ø·ÖĄė£¬ÅØĮņĖįµÄĆܶȱČ1-ä嶔Ķé“ó£»
£Ø5£©ĻČŌŚ¼īŠŌĢõ¼žĻĀĖ®½ā£¬ŌŁÓĆĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ¼ģŃ飮
½ā“š ½ā£ŗ£Ø1£©äå»ÆÄĘÓėÅØĮņĖįµĆµ½HBr£¬1-¶”“¼ÓėHBr·¢ÉśČ”“ś·“Ӧɜ³É1-ä嶔Ķ飬×Ü·“Ó¦·½³ĢŹ½ĪŖ£ŗNaBr+H2SO4£ØÅØ£©+CH3CH2CH2CH2OH”śNaHSO4+CH3CH2CH2CH2Br+H2O£¬ÅØĮņĖįÓŠĒæŃõ»ÆŠŌ£¬äåĄė×ÓÓŠ»¹ŌŠŌ£¬²æ·Öäå»ÆĪļ±»Ńõ»Æ³Éä壬µ¼ÖĀ²śĘ·ĶłĶł³Źŗģ×ŲÉ«£¬
¹Ź“š°øĪŖ£ŗNaBr+H2SO4£ØÅØ£©+CH3CH2CH2CH2OH”śNaHSO4+CH3CH2CH2CH2Br+H2O£»ÅØĮņĖįÓŠĒæŃõ»ÆŠŌ£¬äåĄė×ÓÓŠ»¹ŌŠŌ£¬²æ·Öäå»ÆĪļ±»Ńõ»Æ³Éä壻
£Ø2£©Ēæ¼īČŻŅ׏¹1-ä嶔ĶéĖ®½ā£¬äå¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉŅŌÓĆ»¹ŌŠŌµÄNaHSO3ČÜŅŗ³żČ„£¬·“Ó¦Ąė×Ó·½³ĢĪŖ£ŗBr2+HSO3-+H2O=3H++SO42-+2Br-£¬
¹Ź“š°øĪŖ£ŗc£»Br2+HSO3-+H2O=3H++SO42-+2Br-£»
£Ø3£©Ģ¼ĖįĒāÄĘČÜŅŗĪŖČõ¼ī£¬×īŹŹŅĖ³żČ„Ź£ÓąµÄĮņĖį£¬ĒāŃõ»ÆÄĘČÜŅŗ¼īŠŌĢ«Ē棬ŃĒĮņĖįĒāÄĘČÜŅŗ·“Ó¦»įÉś³É¶žŃõ»ÆĮņĘųĢ壬äå»ÆÄĘČÜŅŗÓėÉŁĮæĮņĖį²»·“Ó¦£¬
¹ŹŃ”£ŗb£»
£Ø4£©ÅØĮņĖįÓėÓŠ»śĪļ²»»„ČÜ£¬²ÉÓĆ·ÖŅŗ·½·Ø·ÖĄė£¬ŠčŅŖÓĆ·ÖŅŗĀ©¶··ÖĄė£¬ÅØĮņĖįµÄĆܶȱČ1-ä嶔Ķé“ó£¬ÓŠ»ś²ćŌŚÉĻ²ć£¬
¹Ź“š°øĪŖ£ŗ·ÖŅŗĀ©¶·£»ÉĻ£»
£Ø5£©¼ģŃé²śĪļÖŠŗ¬ÓŠäåŌŖĖŲµÄŹµŃé·½·ØŹĒ£ŗȔɣĮæ²śĘ·ŃłĘ·£¬¼ÓČėNaOHČÜŅŗ²¢¼ÓČČ£¬ÓĆĻ”ĻõĖįµ÷ÖĮĖįŠŌ£¬¼ÓČėĻõĖįŅųČÜŅŗ£¬²śÉśµ»ĘÉ«³Įµķ£¬
¹Ź“š°øĪŖ£ŗȔɣĮæ²śĘ·ŃłĘ·£¬¼ÓČėNaOHČÜŅŗ²¢¼ÓČČ£¬ÓĆĻ”ĻõĖįµ÷ÖĮĖįŠŌ£¬¼ÓČėĻõĖįŅųČÜŅŗ£¬²śÉśµ»ĘÉ«³Įµķ£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļÖʱøŹµŃ飬¹Ų¼üŹĒ¶ŌŌĄķµÄĄķ½ā£¬²ąÖŲæ¼²éĪļÖŹµÄ·ÖĄėĢį“æµČ£¬³żŌÓ֊עŅāĒæ¼īČŻŅ×µ¼ÖĀĀ±“śĢžĖ®½ā£¬ÕĘĪÕĀ±“śĢžÖŠĀ±ĖŲµÄ¼ģŃé·½·Ø£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ź±¼ä/min | 20 | 40 | 60 | 80 |
| n£ØO2£©/mol | 0.0020 | 0.0032 | 0.0040 | 0.0040 |
| A£® | Ē°20minµÄ·“Ó¦ĖŁĀŹv£ØH2O£©=2.5”Į10-5mol•L-1•min-1 | |
| B£® | “ļĘ½ŗāŹ±£¬ÖĮÉŁŠčŅŖ“ÓĶā½ēĪüŹÕµÄÄÜĮæĪŖ0.968kJ | |
| C£® | Ōö“óc£ØH2O£©£¬æÉŅŌĢįøßĖ®µÄ·Ö½āĀŹ | |
| D£® | Ź¹ÓĆÄÉĆ×¼¶Cu2OæÅĮ£ŹĒĪŖĮĖĢįøߓ߻Ɗ§¹ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«ĀČĘųĶØČėĖ®ÖŠ£ŗCl2+H2O?2H++Cl-+ClO- | |
| B£® | Ģ¼ĖįøĘČÜÓŚ“×Ėį£ŗCaCO3+2H+ØTCa2++CO2”ü+H2O | |
| C£® | ĢśÓėFeCl3ČÜŅŗ·“Ó¦£ŗFe+Fe3+ØT2Fe2+ | |
| D£® | ĮņĖįČÜŅŗÓėĀČ»Æ±µČÜŅŗ»ģŗĻ£ŗBa2++SO42-ØTBaSO4”ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.5mol•L-1CuCl2ČÜŅŗŗ¬ÓŠ3.01”Į1023øöCu2+ | |
| B£® | 28g¾ŪŅŅĻ©·Ö×Óŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ NA | |
| C£® | 0.2mol PCl5·Ö×ÓÖŠ£¬¼üŹżÄæĪŖNA | |
| D£® | ±ź×¼×“æöĻĀ£¬3.36L H2Oŗ¬ÓŠ9.03”Į1023øöH2O·Ö×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
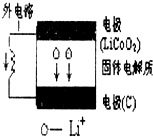
| A£® | µē³ŲÄŚ²æ”°”ś”±±ķŹ¾·ÅµēŹ±Li+µÄĒØŅĘ·½Ļņ£¬ĶāµēĀ·ÉĻµÄ”°”ś”±±ķŹ¾·ÅµēŹ±µÄµēĮ÷·½Ļņ | |
| B£® | ·ÅµēŹ±øŗ¼«µÄµē¼«·“Ó¦£ŗLiCoO2-xe-ØTLi1-xCoO2+xLi+ | |
| C£® | ³äµēŹ±Ņõ¼«µÄµē¼«·“Ó¦£ŗ6C+xLi++xe-ØTLixC6 | |
| D£® | µ±ĶāµēĀ·ÓŠ2 mole-Ķعż£¬·¢ÉśĒØŅʵÄLi+µÄÖŹĮæĪŖ7 g£ØLiµÄĻą¶ŌŌ×ÓÖŹĮæĪŖ 7£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com