
【题目】在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示。下列说法不正确的是
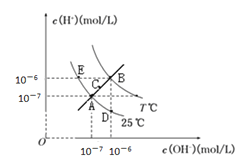
A. 图中五点Kw间的关系:B>C>A=D=E
B. 在温度不变的水中,加入适量的NH4Cl,无法实现从A点变到C点
C. D点对应的水溶液中,可能有NH4+、Fe3+、Cl-、NO3-大量同时存在
D. 若处在B点时,将pH =2的硫酸溶液与 pH = 10的KOH溶液等体积混合,所得溶液呈中性
【答案】C
【解析】
A.通过关系式:KW= c(H+)![]() c(OH-)可计算出图中五点关系:B点KW =10-6
c(OH-)可计算出图中五点关系:B点KW =10-6![]() 10-6=10-12,A、D、E在同一条曲线上,所以三点的KW相等,KW=10-7
10-6=10-12,A、D、E在同一条曲线上,所以三点的KW相等,KW=10-7![]() 10-7=10-14,C点位于A、B之间,所以10-14<KW<10-12, B>C>=A=D=E, 故A正确;B.AC这条直线表示的是c(H+)
10-7=10-14,C点位于A、B之间,所以10-14<KW<10-12, B>C>=A=D=E, 故A正确;B.AC这条直线表示的是c(H+)![]() c(OH-),这条直线只与水溶液的温度变化有关,与其它因素无关,而且温度不变时,加入NH4Cl会使c(H+)增大,c(OH-减小,无法实现从A点变到C点,故B正确;C. D点对应的水溶液中,c(H+)
c(OH-),这条直线只与水溶液的温度变化有关,与其它因素无关,而且温度不变时,加入NH4Cl会使c(H+)增大,c(OH-减小,无法实现从A点变到C点,故B正确;C. D点对应的水溶液中,c(H+)![]() c(OH-)显碱性,不可能和NH4+、Fe3+大量共存,故C错误;D.B点处KW =10-6
c(OH-)显碱性,不可能和NH4+、Fe3+大量共存,故C错误;D.B点处KW =10-6![]() 10-6=10-12,所以pH=6时溶液呈中性,将pH=2的硫酸溶液与pH=10的KOH溶液等体积混合,pH=6,所得溶液呈中性,故D项正确。答案:C。
10-6=10-12,所以pH=6时溶液呈中性,将pH=2的硫酸溶液与pH=10的KOH溶液等体积混合,pH=6,所得溶液呈中性,故D项正确。答案:C。


科目:高中化学 来源: 题型:
【题目】如图是由常见元素组成的一些单质及其化合物之间的转化关系图。常温常压下,B、E、F、H、I均为气体,F无色无味,且能使澄清石灰水变浑蚀;B、E、I均有刺激性气味,E能使湿润的红色石蕊试纸变蓝,B、E在空气中相遇会产生白烟,I为红棕色。A是一种常见的氮肥,F也能由A直接分解可得到。C、G、K的焰色反应呈黄色。(反应中部分生成物己略去)

请回答下列问题:
(1) 物质D的化学式为______,D的其水溶液中阳离子的检验方法为(文字表述):______。
(2)写出反应③的化学方程式:______
(3)写出反应④的离子方程式:______
(4)写出物质E的电子式:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 黄绿色的氯水光照后颜色变浅
B. 温度过高对合成氨不利
C. 由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
D. 溴水中有平衡:Br2+ H2O![]() HBr+ HBrO,当加入AgNO3溶液后,溶液颜色变浅
HBr+ HBrO,当加入AgNO3溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的一氯代物有两种,二氯代物有四种的是( )
A.CH3CH3B.CH3CH2CH3C.CH3CH2CH2CH3D.(CH3)2CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol·L-1稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是
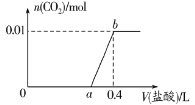
A.在0~a范围内,只发生中和反应
B.a=0.2
C.ab段发生反应的离子方程式为CO32-+2H+=CO2↑+H2O
D.原混合溶液中NaOH与Na2CO3的物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
(1)已知CO(g)、H2(g)的标准燃烧热分别为 △H=-283kJmol-1, △H=-286kJmol-1,且CH3OH(g)+3/2O2(g) ![]() CO2(g)+2H2O(l) △H=-761kJmol-1;则CO(g)+ 2H2(g)
CO2(g)+2H2O(l) △H=-761kJmol-1;则CO(g)+ 2H2(g)![]() CH3OH(g)的△H= ___________。
CH3OH(g)的△H= ___________。
(2)为了提高CO和H2制备甲醇生产效率和产量;工业生产中通常采取的措施是___________________________________________。(写出两点)
(3)实验室模拟用CO和H2反应来制甲醇,在250 ℃下,将一定量的CO和H2投入10 L的密闭容器中,各物质的物质的量浓度(mol·L-1)变化如下表所示:
2 min | 4 min | 6 min | |
CO | 0.07 | 0.05 | 0.05 |
H2 | x | 0.10 | 0.10 |
CH3OH | 0.03 | 0.05 | 0.05 |
①250 ℃时,该反应的平衡常数K=___________;
②在图1中画出反应开始至第6 min时H2的物质的量的变化曲线,并标出合适的纵坐标。_______
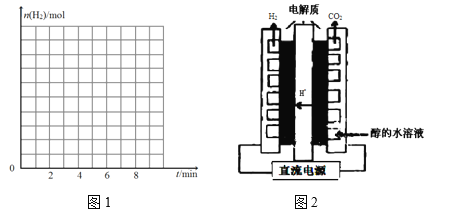
(4)利用电解甲醇水溶液制备氢气最大的优点就是需要的电压低,装置如图2,写出 阳极电极反应方程式____________________________________________________,电解的总反应化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁与铜的粉末按物质的量之比为2︰1的比例混合均匀,取出mg混合物,投入到100mL 3mol·L-1FeCl3溶液中,充分反应(反应后溶液体积变化忽略不计)。试计算:
(1)如果固体完全溶解,则m最大值为____。
(2)如果溶液中Cu2+浓度为0.25 mol·L-1,则m值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究白色固体X(仅含两种元素)的组成和性质,设计并完成如下实验(所加试剂都是过量的):
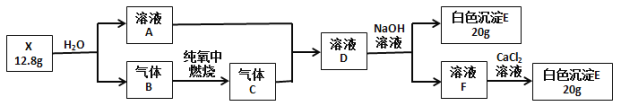
其中气体B在标准状况下的密度为1.16 g·L-1请回答:
(1) X的化学式是________。
(2) 气体B的电子式________。
(3) 溶液D与NaOH溶液反应的离子反应方程式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是( )

A. 离O点越远的元素原子半径越大
B. 虚线相连的元素处于同一族
C. N点代表的是图中金属性最强的元素
D. M、N点代表的元素组成的化合物中可能含有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com