
| A. | 1:3 | B. | 1:7 | C. | 1:6 | D. | 5:3 |
分析 发生反应:C2H4+3O2$\stackrel{点燃}{→}$2CO2+2H2O,120℃时水为气体,反应前后气体的物质的量不变,平均相对分子质量不变,由反应后的相对氢气的密度计算原混合气体中乙烯和氧气的平均相对分子质量,以此计算原混合气体中乙烯和氧气的体积比.
解答 解:发生反应:C2H4+3O2$\stackrel{点燃}{→}$2CO2+2H2O,120℃时水为气体,反应前后气体的物质的量不变,平均相对分子质量不变,
测得反应后的混合气体对H2的相对密度是15.75,则原混合气体的平均相对分子质量为15.75×2=31.5,
设混合气体中乙烯为x,氧气为y,则
$\frac{28x+32y}{x+y}$=31.5,
解得x:y=1:6,
故选C.
点评 本题考查有机反应的计算,为高频考点,把握发生的反应及平均相对分子质量的计算为解答的关键,侧重分析与计算能力的考查,注意120℃乙烯的燃烧反应前后体积不变,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该食盐中一定没有添加KIO3 |
| D | 向苯酚钠溶液中滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性一定比苯酚强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③④⑥ | C. | ①③④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
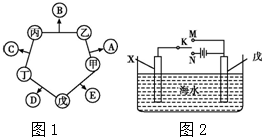 甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图1所示.又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是应用最广泛的金属.②乙在甲中
甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图1所示.又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是应用最广泛的金属.②乙在甲中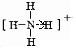 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
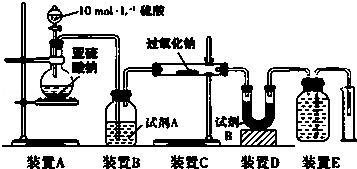
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 强电解质 | 弱电解质 | 酸性氧化物 | 碱性氧化物 | |
| A | H2SO4 | CH3COOH | NO2 | Na2O |
| B | BaSO4 | HClO | Mn2O7 | CaO |
| C | NaCl | 氨水 | SO2 | MnO2 |
| D | HI | HF | CO2 | Fe3O4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 282.8 kJ/mol | B. | -282.8 kJ/mol | C. | 848.4kJ/mol | D. | -848.4 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Na+、Br- | B. | NH4+、Na+、AlO2- | C. | Ba2+、Al3+、Cl- | D. | K+、MnO4-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com