
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O===Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O
科目:高中化学 来源:2014-2015学年甘肃省张掖市高三4月诊断考试理综化学试卷(解析版) 题型:简答题
【化学——选修2:化学与技术】(15分)将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是________(填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁等的提取工艺
(2)采用“空气吹出法”从浓海水吹出Br2,并用纯碱吸收。溴歧化为Br-和BrO3-并没有产生CO2则反应的离子反应方程式为 。
(3)海水提镁的一段工艺流程如下图:
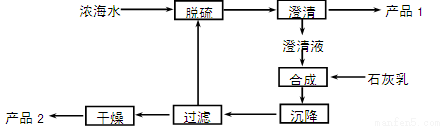
浓海水的主要成分如下:
离子 | Na+ | Mg2+ | Cl- | SO42- |
浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的阳离子_______,获得产品2的离子反应方程式为 ,浓海水的利用率为90%,则1 L浓海水最多可得到产品2的质量为________g。
(4)由MgCl2·6H2O制备MgCl2时,往往在HCl的气体氛围中加热。其目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:选择题
下列各组化合物中,不论二者以何种比例混合,只要总质量一定,则完全燃烧时消耗O2和生成的H2O的质量不变的是
A.C2H2 C6H6 B.C2H6 C3H6
C.C2H4 C3H4 D.C2H4 C2H5OH
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省宝鸡市高二4月月考化学试卷(解析版) 题型:选择题
下列表示的是正丙基的是
A.CH3CH2CH3 B.CH3 CH2CH2-
C.―CH2CH2CH2― D.(CH3 )2CH-
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
为了配制NH4+浓度与Cl-的浓度比为1:1的溶液,可在NH4Cl溶液中加入①适量的HCl②适量的NaCl③适量的氨水④适量的NaOH,正确的是
A.①② B.③ C.③④ D.④
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
对于反应2SO2+O2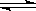 2SO3,下列判断正确的是
2SO3,下列判断正确的是
A.2体积2SO2和足量O2反应,必定生成2体积SO3
B.其他条件不变,增大压强,平衡必定向左移动
C.平衡时,SO2消耗速率必定等于O2生成速率的两倍
D.平衡时,SO2浓度必定等于O2浓度的两倍
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列用来表示物质变化的化学用语中,正确的是
A.钢铁发生电化学腐蚀的正极反应式:Fe-2e-= Fe2+
B.HS-水解的离子方程式:HS-+H2O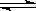 S2-+H3O+
S2-+H3O+
C.CO32-水解的离子方程式:CO32-+2 H2O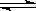 H2CO3 +2OH-
H2CO3 +2OH-
D.用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+ Hg2+(aq)=HgS(s)+Fe2+(aq)
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省德阳市高一下学期第一次月考化学试卷(解析版) 题型:选择题
Se是人体必需微量元素,下列关于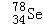 和
和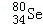 的说法正确的是
的说法正确的是
A.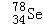 和
和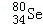 互为同素异形体
互为同素异形体
B.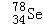 和
和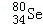 互为同位素
互为同位素
C.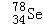 和
和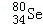 分别含有44和46个质子
分别含有44和46个质子
D.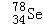 和
和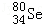 都含有34个质子和中子
都含有34个质子和中子
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高二下学期第一次月考化学试卷(解析版) 题型:填空题
(16分)
(1)有9种微粒:①NH2-;②—NH2;③Br-;④OH-;⑤—NO2;⑥—OH;⑦NO2;⑧CH3+;⑨—CH3.属于官能团的有(填序号)___ _____ 。
(2)有下列8种晶体,用序号回答下列问题:
A.水晶
B.冰
C.白磷
D.固态氩
E.氯化铵
F.铝
G.金刚石
①属于原子晶体是 ,直接由原子构成的分子晶体是 _____ 。
②由极性分子构成的分子晶体是 ,含有共价键的离子晶体是 _____ 。
③在一定条件下能导电而不发生化学反应的是 _____。
分子内存在化学键,但受热熔化时,化学键不发生变化的是 _____。
(3)在NaCl晶胞中8个顶点 、6个面心处各有一个Na+ ,12条棱的中点、体心各有一个Cl- ,KCl和NaCl的晶格型式相同。已知Na+离子的半径是Cl-离子的0.5倍,是K+离子的0.7 倍,计算:KCl晶胞和NaCl晶胞的边长之比为 _____ 。
(4)如下图:由正五边形构成的多面体有20个顶点,多面体中有_____个正五边形,共有____条棱边.
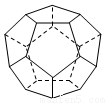
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com