
| ��ʯ���� | ��ͭ�� | ��ͭ�� | ��ͭ�� | ��ȸʯ |
| ��Ҫ�ɷ� | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3?Cu��OH��2 |
| ||
| ѡ�� | ������ | ������ | �ж� |
| A | ͭ�̵����ɷ��Ǽ�ʽ����ͭ | ����ϡ�����ͭ�������ͭ�� | ��ԣ���ԣ��� |
| B | ͭ�����γ����ܵ�����Ĥ | ͭ��������ʢ��Ũ���� | ��ԣ���ԣ��� |
| C | ����ͭ���� | í��ͭ���ϵ������ڳ�ʪ�����в������� | ��ԣ���ԣ��� |
| D | ��ɫ����ͭ��������ת��Ϊ��ɫ����ͭ��ĩ�������仯 | ����ͭ��Һ��������Ӿ�ص������� | �������ԣ��� |
| ͭ��ԭ������ԭ�Ӹ��� |
| ������ |
| ͭ��ԭ������ԭ�Ӹ��� |
| ������ |
| 64 |
| 64+56+32��2 |
| 64��5 |
| 64��5+56+32��4 |
| 64��2 |
| 64��2+32 |
| 64��2 |
| 64��2+12+16��5+1��2 |
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������е�����������Һ�������е���Ԫ�أ�Ag++Br-=AgBr�� | ||||
| B��14g��ϩȼ������Һ̬ˮ����b kJ���������ʾ��ȼ���ȵ��Ȼ�ѧ����ʽΪ��C2H4��g��+3 O2��g���T2 H2O��g��+2 CO2��g����H=-2 b kJ?mol-1 | ||||
C���ö��Ե缫��ⱥ��KCl��Һ��2 H++2 Cl-
| ||||
| D������������˫��ˮ��ϡH2SO4��ϣ�2 Fe2++H2O2+2 H+=2 Fe3++2 H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
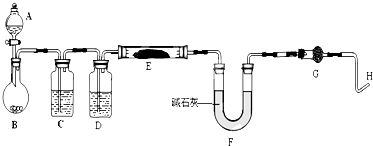
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���K NO3 ���壬ͭ���Բ��ܽ� |
| B���������ʵ���Cl2��SO2ͨ��Ʒ����Һ��Ư������ǿ |
| C��ŨH2SO4��Cu��C��Ӧ������ȣ�Ũ������Cu��C��Ӧ��������� |
| D��������������С�մ���臨���������������������������Һ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£�ij�������KspΪ2.5��105 | ||||
| B����Ӧ2Mg��s��+CO2��g��=C��s��+2MgO��s�����Է����У���÷�Ӧ�ġ�H��0 | ||||
C��NH3?H2O��Һ��ˮϡ�ͺ���Һ��
| ||||
| D�������£�pH��Ϊ5���������Ȼ����Һ�У�ˮ�ĵ���̶���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
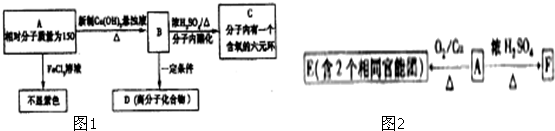
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��11.2LH2��0.5molCO2 |
| B��18mLH2O��4�棩��2��105Pa��27��32gO2 |
| C��1molCO��88gCO2 |
| D��27�棬22.4LCl2�ͺ�4mol��ԭ�ӵ�H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��21.6 | B��28 |
| C��14 | D��31 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com