
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A.标准状况下,22.4L CCl4含有的分子数为1NA
B.通常状况下,NA个CO2分子占有的体积为22.4L
C.常温常压下,1.06g Na2CO3溶于水,溶液中含Na+离子数为0.02NA
D.浓度为0.5mol/L的MgCl2溶液中,含有Cl数为NA个
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某有机物结构简式为 ,下列叙述不正确的是( )
,下列叙述不正确的是( )
A. 1 mol 该有机物在加热和催化剂作用下,最多能和4 mol H2反应
B. 该有机物能使溴水褪色,也能使酸性KMnO4溶液褪色
C. 该有机物遇硝酸银溶液产生白色沉淀
D. 该有机物在一定条件下能发生消去反应或取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究氢氧化铝的两性,最适宜的试剂是( )
A.AlCl3、氨水、稀盐酸B.![]() 、氨水、稀盐酸
、氨水、稀盐酸
C.Al、NaOH溶液、稀盐酸D.![]() 溶液、NaOH溶液、稀盐酸
溶液、NaOH溶液、稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是( )
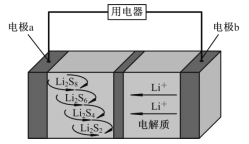
A. 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
B. 电池工作时,外电路中流过 0.02 mol 电子,负极材料减重 0.14 g
C. 石墨烯的作用主要是提高电极a的导电性
D. 电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是某工业生产过程。

溶解度表:
温度℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
氯化铵 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 65.6 | 71.3 | 77.3 |
硫酸铵 | 70.6 | 73 | 75.4 | 78 | 81 | 88 | 95 | 98 | 103 |
硫酸钾 | 7.4 | 9.3 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 22.9 | 24.1 |
氯化钾 | 28 | 31.2 | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 53.9 | 56.3 |
(1)本工业生产过程的目标产品是____________________________________。(写化学式)
(2)过滤Ⅰ操作所得固体中,除CaCO3外还有一种物质,该固体的用途有_________(试举一例)。
(3)根据溶解度表转化Ⅱ适宜的温度是________
A、0~10℃ B、20~30℃ C、40~60℃ D、90~100℃
过滤Ⅱ操作所得滤渣是__________。
(4)我国著名的化学家也利用了转化Ⅱ的反应原理制备了一种重要的碱,该制备的化学反应方程式为:___________________________________________________
(5)氯化钙结晶水合物(CaCl2·6H2O)进行脱水处理可制得常用的干燥剂,根据下图选择最佳脱水的方法是__________

A、氯化氢气流中加热到174℃ B、直接加热至174℃
C、直接加热至260℃ D、氯化氢气流中加热到260℃
(6)上述工业流程实现了绿色化学的理念,其中__________________(填化学式)实现了循环利用,副产品_________________________(填化学式)可转化为原料,整个流程基本实现了污染物零排放。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是l mol金属镁和卤素反应的△H(单位:kJ· mol-1)示意图,反应物和生成物均为常温时的稳定状态,下列选项中不正确的是
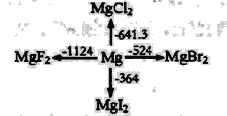
A.由图可知,MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJ· mol-1
B.MgI2与Br2反应的△H<0
C.电解MgBr2制Mg是吸热反应
D.化合物的热稳定性顺序:MgI2>MgBr2>MgCl2>MgF2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个2 L恒容的容器中,分别发生反应A(g)+3B(g)![]() 2C(g),5min后各容器反应达平衡状态,其中甲容器中A的物质的量为0.4 mol。下列说法正确的是()
2C(g),5min后各容器反应达平衡状态,其中甲容器中A的物质的量为0.4 mol。下列说法正确的是()
反应前各物质的物质的量/mol
A | B | C | |
甲 | 1 | 3 | 0 |
乙 | 0 | 0 | 2 |
丙 | 1.5 | 4.5 | 1 |
A.乙中5min内C的反应速率为0.16mol-1·min-1
B.达到平衡时,丙中A的浓度是甲中的2倍
C.丙中反应的平衡常数大于甲中反应的平衡常数
D.达到平衡时,甲、乙两容器中C的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,科学家已经研制出世界上最薄的材料——碳膜片,其厚度只有一根头发的二十万分之一。如图所示,这种碳膜片形状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )

A. 碳膜片属于一种新型的化合物
B. 碳膜片与石墨的结构相同
C. 碳膜片与C60互为同素异形体
D. 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物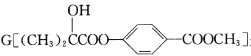 是一种医药中间体,它的一种合成路线如下:
是一种医药中间体,它的一种合成路线如下:
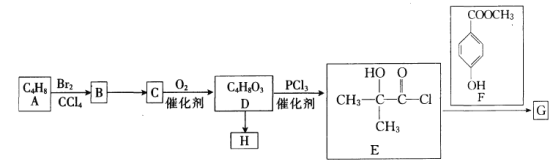
已知:![]() 。请回答下列问题:
。请回答下列问题:
(1)A的化学名称是______________,G的分子式为____________________。
(2)由B生成C的反应条件为____________,由E和F生成G的反应类型是___________。
(3)D在浓硫酸/加热条件下会反应生成一种含六元环的化合物,该化合物的结构简式为______________。
(4)H是一种高聚酯。D生成H的化学方程式为__________________________________。
(5)符合下列要求的F的同分异构体共有___________种。
①苯环上有三个取代基;②能发生银镜反应;③1mol该物质能与2molNa2CO3反应。
请写出其中能与足量浓溴水反应,所得产物的苯环上不存在氢原子的F的同分异构体结构简式:_______________________(任写一种)。
(6)已知酚羟基不易与羧酸发生酯化反应,写出以苯酚、甲苯为原料制备苯甲酸苯酯![]() 的合成路线(其他无机试剂任选):____________。
的合成路线(其他无机试剂任选):____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com