
| A、乙醇结构中有-OH,其水溶液可以电离出OH-而显碱性 |
| B、乙醇与乙酸在一定条件下反应生成乙酸乙酯 |
| C、乙醇与钠反应可以产生氢气,所以乙醇显酸性 |
| D、乙醇与钠反应比较平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼 |


科目:高中化学 来源: 题型:
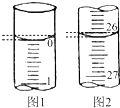 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L 盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | ① | ② |
| 第二次 | 25.00 | 1.56 | 27.68 | 26.12 |
| 第三次 | 25.00 | 0.22 | 26.30 | 26.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、应该使用萃取的方法,并选用酒精作萃取剂 |
| B、萃取使用的主要仪器是分液漏斗,在使用前要先检验其是否漏液 |
| C、静置分层后碘单质一定溶在上层液体中,应从分液漏斗的上口倒出 |
| D、从分液漏斗中分离出的就是纯净的碘单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位时间内生成nmolA2,同时消耗2n molAB |
| B、容器内,3种气体AB、A2、B2共存 |
| C、容器的总压强不变 |
| D、容器中各组分的体积分数不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 结构简式 | 沸点/℃ | 相对密度 |
| ① | CH3Cl | -24.2 | 0.915 9 |
| ② | CH3CH2Cl | 12.3 | 0.897 8 |
| ③ | CH3CH2CH2Cl | 46.6 | 0.890 9 |
| ④ | CH3CHClCH3 | 35.7 | 0.861 7 |
| ⑤ | CH3CH2CH2CH2Cl | 78.44 | 0.886 2 |
| ⑥ | CH3CH2CHClCH3 | 68.2 | 0.873 2 |
| ⑦ | (CH3)3CCl | 52 | 0.842 0 |
| A、物质①②③⑤可互相称为同系物 |
| B、一氯代烷同分异构体的沸点随着支链的增多而升高 |
| C、一氯代烷的沸点随着碳数的增多而趋于升高 |
| D、一氯代烷的相对密度随着碳数的增多而趋于减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、①④表现出酸性 |
| B、①②表现出氧化性 |
| C、③既表现出氧化性又表现出酸性 |
| D、③④表现出还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、常温下,将pH=11的氨水和pH=3的盐酸,等体积混合后,所得溶液中各离子浓度的关系是c(Cl-)>c(NH
| ||
| B、某二元酸在水中的电离方程式为:H2B═H++HB-,HB-?H++B2-,所以NaHB溶液呈酸性 | ||
| C、在BaSO4饱和溶液中加入少量的BaCl2溶液产生沉淀,平衡后的溶液中:C(Ba2+)?C(SO42-)>Ksp;c(Ba2+)>C(SO42-) | ||
| D、等浓度的NH3?H2O、NH4HSO4,NH4Cl溶液中c(NH4+)在逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、OH-、Cl-、HCO3- |
| B、H+、Na+、Fe2+、MnO4- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、NH4+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大于40% | B、等于40% |
| C、小于40% | D、无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com