
һ�������£�ͨ�����з�Ӧ�����Ʊ������մɵ�ԭ��MgO��MgSO4(s)��CO(g)MgO(s)��CO2(g)��SO2(g)����H��0
�÷�Ӧ�ں��ݵ��ܱ������дﵽƽ��������ı�ͼ�к�����x��ֵ�����´ﵽƽ���������y��x�仯���ƺ������� (����)��

| ѡ�� | x | y |
| A | �¶� | �����ڻ��������ܶ� |
| B | CO�����ʵ��� | CO2��CO�����ʵ���֮�� |
| C | SO2��Ũ�� | ƽ�ⳣ��K |
| D | MgSO4������(�������) | CO��ת���� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ͼ2�е����ʲ��䵽ͼ1�У��ɵõ�һ��������������ԭ�����ӷ���ʽ(δ��ƽ)��
 ����
����
ͼ1
 ��
�� ��
�� ��
�� ��
��
ͼ2
���ڸ����ӷ���ʽ��˵������ȷ���� (����)��
A��IO ��������
��������
B�������ԣ�Mn2��>IO
C���������뻹ԭ�������ʵ���֮��Ϊ5��2
D������2 mol Mn2���μӷ�Ӧʱ����ת��10 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ�ҷ���ijҩ��M��������Ѫ�ܼ�������Ϊ�������������ͷų�һ�֡���ʹ���ӡ�D����������D�������ڵ�����ԭ����
��ش��������⣺
(1)��֪M����Է�������Ϊ227����C��H��O��N����Ԫ����ɣ�C��H��N��������������Ϊ15.86%��2.20%��18.50%����M�ķ���ʽ��____________��D��˫ԭ�ӷ��ӣ���Է�������Ϊ30����D�ķ���ʽ��______________________________��
(2)��֬A����ͼ��ʾ��;���ɵõ�M��



ͼ�Тڵ���ʾΪ��

��Ӧ�ٵĻ�ѧ����ʽ��
________________________________________________________________________��
��Ӧ�ڵĻ�ѧ����ʽ��
(3)C��B��������һ�������·�Ӧ���ɵĻ������Է�������Ϊ134��д��C���п��ܵĽṹ��ʽ�� ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�¶�ʱ��N2��3H22NH3��ƽ�ⳣ��K��a������¶��£�NH3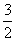 H2��
H2��
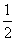 N2��ƽ�ⳣ��Ϊ (����)��
N2��ƽ�ⳣ��Ϊ (����)��
A.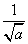 B.
B.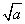 ����
����
C.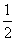 a D.
a D.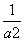
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��Ӧ��2SO2(g)��O2(g)2SO3(g)����H<0��ij�¶��£���2 mol SO2��1 mol O2����10 L�ܱ������У���Ӧ��ƽ���SO2��ƽ��ת����(��)����ϵ��ѹǿ(p)�Ĺ�ϵ��ͼ����ʾ��������˵����ȷ���� (����)��
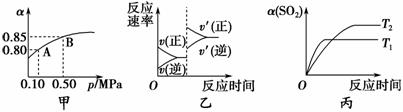
A����ͼ���ƶϣ�B��SO2��ƽ��Ũ��Ϊ0.3 moL��L��1
B����ͼ���ƶϣ�A���Ӧ�¶��µ�ƽ�ⳣ��Ϊ80
C���ﵽƽ�����С�����ݻ�����Ӧ���ʱ仯ͼ�������ͼ�ұ�ʾ
D��ѹǿΪ0.50 MPaʱ����ͬ�¶���SO2��ƽ��ת�������¶ȹ�ϵ��ͼ������T2>T1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�����ܱ������г���һ����SO2��O2���з�Ӧ��2SO2(g)��O2(g)2SO3(g)����H<0����Ӧ����(v)���¶�(T)��SO2���������[V(SO2)%]��ѹǿ(p)�Ĺ�ϵ�ֱ���ͼ�ס�ͼ����ʾ������˵������ȷ���� (����)��

A��ͼ���У�����1��ʾ�淴Ӧ�������¶ȵĹ�ϵ
B��ͼ���У�d���ʾ�¶�ΪT0ʱ����Ӧ�Ѿ��ﵽƽ��
C��ͼ���У��¶Ⱥ㶨ʱ��a��b�����Ӧ�ķ�Ӧ���ʣ�va>vb
D��ͼ���У��¶Ⱥ㶨ʱ��c��ķ�Ӧ�������淴Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������糧�ͷų�����������̼����ȼú����������̼�ȴ�������ʵ����ɫ���������ܼ��š��������õ�Ŀ�ġ���CO2ת��Ϊ�״���һ��������̼�������䷴ӦΪCO2(g)��3H2(g)CH3OH(g)��H2O(g)����H��
(1)ȡ��ݵ������CO2��H2�Ļ������(���ʵ���֮�Ⱦ�Ϊ1��3)���ֱ�����¶Ȳ�ͬ���ݻ���ͬ�ĺ����ܱ������У�����������Ӧ����Ӧ��ͬʱ���ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ������ͼ����ʾ��������CO2ת��Ϊ�״��ķ�Ӧ�Ħ�H________0(�>������<������)��
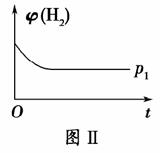

(2)��ͼ�����ں����ܱ������У�ѹǿΪp1ʱH2�����������ʱ��t�ı仯���ߣ�����ͼ�л����÷�Ӧ��p2(p2>p1)ʱH2�� ���������ʱ��t�ı仯���ߡ�
(3)��һ���º����ܱ������г���1 mol CO2��3 mol H2������������Ӧ�����CO2��CH3OH(g)�����ʵ���Ũ����ʱ��ı仯��ͼ����ʾ��

��0��10 min�ڣ�������ƽ����Ӧ����Ϊ________�����¶��£���Ӧ��ƽ�ⳣ��Ϊ________(������λ��Ч����)��10 min������������ٳ���1 mol CO2��3 mol H2�����ٴδﵽƽ��ʱCH3OH(g)���������________(���������С�����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ijͬѧ�����ڳ��ȵ�ú̿��������ˮ��ú¯�л��������ɫ�Ļ��棬¯���������˸�ͬѧ�ó����ۡ�ú̿ȼ��ʱ������ˮ����ʹú̿ȼ��ʱ�ų����������������֪��ú̿��ȼ����Ϊ 393.15 kJ �� mol��1 ��������ȼ����Ϊ 242 kJ�� mol��1 ��һ����̼��ȼ����Ϊ 283 kJ �� mol��1 �������й�˵����ȷ����
A����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ 2H2(g)�� O2(g)===2H2O (l) ����H�� ��242 kJ �� mol��1
B����ʾCO ȼ���ȵ��Ȼ�ѧ����ʽΪ 2CO(g)�� O2(g)===2CO2 (g) ����H�� �� 566 kJ �� mol��1
C����¯�����������Ϊ�����Ĺ���ú̿ת��Ϊ��ȼ������
D���� 242 kJ��mol��1 ��283 kJ�� mol��1 ��393.15 kJ��mol��1 ���ʸ�ͬѧ�Ľ����ǶԵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��Ԥ�Գ���ԭ�ӵķ��ֽ����ؽ����ڱ���2005��1��������ѧ���ڡ�Science���Ϸ������ģ�����������A1�ij�ԭ�ӽṹA113��A114�����������Ǽ��ȶ���A113Iһ�ȣ�Al13��Al14�����ʺ����������ڱ��е�ij����Ԫ�أ���֪���೬ԭ�ӵ�����40���۵���ʱ���ȶ�(��Alԭ�Ӿ���3���۵���)������˵������ȷ����
A. Al14��42���۵��ӣ�����IIA��Ԫ����������
B. Al13��39���۵��ӣ�����±����������
C. Al13����������HI��Ӧ������H Al13I���һ�ѧ
����ʽΪ AI13+HI=H AI13I
D. Al13ԭ����A1ԭ�Ӽ���ͨ�����Ӽ���ϵ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com