
�������ӷ���ʽ��д��ȷ����
A��̼�������Һ��������������Һ��ϣ�Ca2++2HCO3����OH����CaCO3��+CO32����H2O
B��CuCl2��Һ��Na2S��Һ2:1��Ӧ��Cu2++ S2��= CuS��
C����Ũ�����ữ��KMnO4��Һ��H2O2��Ӧ��֤��H2O2���л�ԭ�ԣ�2MnO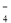 + 6H+ + 5H2O2 �� 2Mn2+ + 5O2�� + 8H2O
+ 6H+ + 5H2O2 �� 2Mn2+ + 5O2�� + 8H2O
D����������Һ�еμ�Ba(OH)2��Һ��ǡ��ʹSO42-������ȫ��2Al3++3SO42-+3Ba2++6OH -=2 Al(OH)3��+3BaSO4��
B
��������
���������A��̼�������Һ��������������Һ���ӦΪ��Ca2++HCO3����OH����CaCO3��+H2O������B��CuCl2��Һ��Na2S��Һ2:1��Ӧ��Cu2++ S2��= CuS������ȷ��C��KMnO4��Һ������Ũ�����ữ�����߷�����Ӧ�����Ȼ��ء����Ȼ��̡�������ˮ������D����������Һ�еμ�Ba(OH)2��Һ��ǡ��ʹSO42-������ȫӦΪ��Al3++2SO42-+2Ba2++4OH -= [Al(OH)4]��+BaSO4��������
���㣺�������ӷ���ʽ�����жϡ�


 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�����л�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
θ�ᣨ���ᣩ����IJ��˳��������к������ҩ�������ƣ��������������ʵ�ҩƷ�ﲻ������Ч��
A��Al(OH)3 B��CaCO3 C��NaHCO3 D��C6H12O6(������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���������NaHCO3��Һ��Ӧ���������������
A���� B���� C���� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ������ѧ�ڵ��Ĵ��¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���й����л����������ȷ����
A�����顢��ϩ�ͱ�����ͨ��ʯ�ͷ���õ�
B���������ϩ�ֱ���Cl2��Ӧ���ж�����������
C����ȩ������(NH4)2SO4��Һ����ʹ�����ʷ�������
D���۱�ϩ�Ľṹ��ʽΪ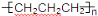
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����������и�����ѧ�ڵ������¿������Ծ��������棩 ���ͣ������
(14��)������Ϊһ���ִ���ͨ�������ڽ���ǧ��������β���к���CO��NOx���ж����壬����Ⱦ����Ҳ��Ϊ������ἱ���������⡣
��1����������������ʱ������N2��O2��Ӧ���������仯ʾ��ͼ��ͼ��
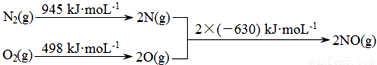
��÷�Ӧ���Ȼ�ѧ����ʽΪ ��
��2����������װβ������װ�ã���ʹCO��NOx�ж��������Ӧת��Ϊ�����塣
2xCO��2NOx == 2xCO2��N2����ת�Ƶ������ʵ���Ϊ0.4x molʱ���÷�Ӧ���ɱ�״���µ�N2��� L��
��3��һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϡ����Ի�ԭ��������������������ϳɺܶ��л�����״��ȡ���ѹǿΪ0.1 MPa�����£���a mol CO��3a mol H2�Ļ�������ڴ��������·�Ӧ���ɼ״��� CO(g)��2H2(g)  CH3OH(g)����H�� -b kJ?mol-1
CH3OH(g)����H�� -b kJ?mol-1
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ ��
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ��� ��
A�������¶� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���1 mol CO��3 mol H2
�۾��ⶨ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����£�
�¶ȣ��棩 | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
��ijʱ�̡�250���ø÷�Ӧ�ķ�Ӧ�����������Ũ��Ϊc(CO) ��0.4 mol/L��c(H2)��0.4 mol/L��c(CH3OH)��0.8 mol��L��1, ���ʱv�� v��(�������)��
��4���״�����Ҫ�Ļ�������ԭ�ϣ�����һ�����͵�ȼ�ϣ��������������һ��ȼ�ϵ�أ�һ���缫ͨ���������һ���缫����״�����صĵ�����Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2-���ӡ��õ�ص�������ӦʽΪ_____________________________����ع���ʱ�������������O2-��_______���ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ������
��14�֣��ӵ�ʳ���к��еĵ������һ�ְ�ɫ�ᾧ��ĩ�������º��ȶ���������560�濪ʼ�ֽ⣬����ص��ܽ�����¶����߱仯���������������µ������һ�ֽ�ǿ��������������⻯��������εȻ�ԭ�����ʷ�Ӧ����ҵ��������ص��������£�
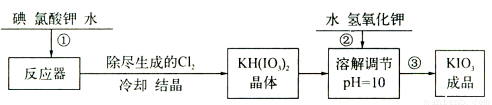
��1����������������ص���Ҫ������ ��
��2�������±�����ص��ܽ�ȣ������۵õ�����ؾ��壬�ɾ��� �����ˡ�ϴ�ӡ�����Ȳ��衣
��3����֪��KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O�� I2+2S2O32-=2I-+S4O62-
Ϊ�˲ⶨ�ӵ�ʳ���е�ĺ�����ijѧ�����������ʵ�飺ȷ��ȡwgʳ�Σ�����������ˮʹ����ȫ�ܽ⣻����ϡ�����ữ������Һ���������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��������ָʾ���������ʵ���Ũ��Ϊ2.00��10-3mol��L-1��Na2S2O3��Һ�ζ�������10.00mLʱǡ�÷�Ӧ��ȫ��
���ڵζ������У����õIJ�������Ϊ �� ��
�ڸ�ʵ������� ��ָʾ�����ζ��յ�������� ��
�������йظõζ�ʵ���˵������ȷ���� ��
A���ζ�����ʹ��ǰ�������Ƿ�©ˮ����ϴ
B���ζ�ʱ�۾�ע�ӵζ�������ҺҺ��仯
C��Ϊ��Сʵ������������������ˮ��ϴ��ƿ�ڱ�
D���յ����ʱ���ӻᵼ�µ�ĺ���ƫ��
�ܼӵ�ʳ����Ʒ�еĵ�Ԫ�غ����� g��kg-1���Ժ�w�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A����֪ ����Լ���CH3��CH3 �� CH2��CH2��H2����H =��125.6 kJ/mol
����Լ���CH3��CH3 �� CH2��CH2��H2����H =��125.6 kJ/mol
B����˵��NH3���H+������H2Oǿ��NH3+H3O+=NH+4+H2O
C����֪�����Ȼ�ѧ����ʽ��2H2(g)+O2(g) === 2H2O(g) ��H����484kJ/mol����������ȼ����Ϊ��242kJ/mol
D����֪�к���Ϊ��57.4kJ/mol ����NaOH��aq�� ��CH3COOH��aq����CH3COONa��aq����H2O��l������H ����57.4kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�����и���һ��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
(12��)��������(NaNO2)��һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС�����Ʊ�NaNO2���ⶨ��Ʒ���ȡ�
I���������ϡ�
��2NO+Na2O2=2NaNO2��2NO2+Na2O2=2NaNO3��
��NO�ܱ����Ը������������NO2��
������������MnO4-����ԭΪMn2+��
���Ʊ���Ʒ��
������װ����NaNO2(�гֺͼ���װ����ʡ��)��
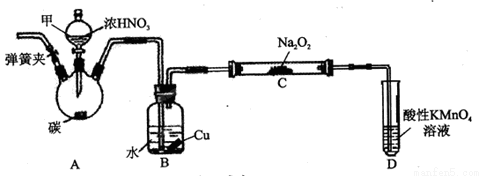
��1��װ��A��ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ_______________________��
��2��Bװ�õ�������_________________________��
��3����ͬѧ��Ϊװ��C�в��ﲻ�����������ƣ�����̼���ƺ��������ƣ�Ϊ�ų�����Ӧ��B��Cװ�ü�����װ��E��E��ʢ�ŵ��Լ�������_________��(����ĸ���)
A��ŨH2SO4 B����ʯ�� C����ˮCaCl2 D����ʯ��
�ⶨ���ȡ���
������·����ⶨ��Ʒ�Ĵ��ȡ�

��4����ҺA����ҺB������Ӧ�����ӷ���ʽΪ____________________________��
��5��ȡ��Ʒ2.3g��һϵ�в�����õ���ҺA100mL��ȷ��ȡ10.00mL A��24.00mL 0.05mol��L������KMnO4��Һ����ƿ�г�ַ�Ӧ����Ӧ����Һ��0.1 mol/L(NH4)2Fe(SO4)2����Һ�ζ�����ɫ�պ���ȥ���ظ�����ʵ��2�Σ�ƽ������(NH4)2 Fe(SO4)2��Һ10.00ml������Ʒ��NaNO2�Ĵ���Ϊ__________��
����̽����˼��
��6��NaNO2�Ĵ���ƫ�ͣ���С�����������ԭ���п�����ȷ����________��(����ĸ���)
A���ζ�����Һ��ɫ�պ���ȥ������ֹͣ�μ�
B������A��KMnO4��Һǰ��ƿδ������
C��ʵ����ʹ�õ�(NH4)2 Fe(SO4)2��Һ��¶�ڿ�����ʱ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡ�����и���12�¼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
(19��) ��1������H2S������ȡ�����ķ����ж��֡�
�ٸ����ȷֽⷨ����֪��H2S(g)  H2(g)+1/2S2(g)��H�ں����ܱ������У����Ʋ�ͬ�¶Ƚ���H2S�ֽ�ʵ�顣��H2S��ʼŨ�Ⱦ�Ϊc mol/L�ⶨH2S��ת���ʣ������ͼ��
H2(g)+1/2S2(g)��H�ں����ܱ������У����Ʋ�ͬ�¶Ƚ���H2S�ֽ�ʵ�顣��H2S��ʼŨ�Ⱦ�Ϊc mol/L�ⶨH2S��ת���ʣ������ͼ��
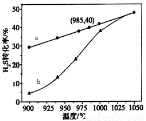
ͼ��aΪH2S��ƽ��ת�������¶ȹ�ϵ���ߣ�b���߱�ʾ��ͬ�¶��·�Ӧ������ͬʱ����δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ���H_____0(���=��)��˵�����¶ȵ����ߣ�����b������a������ԭ��________________________��
�ڵ绯ѧ�����÷�������̵�ʾ��ͼ��ͼ��
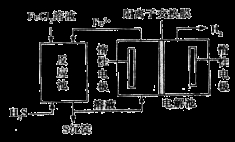
��Ӧ���з�Ӧ�����ӷ���ʽ��_____________________________��
��Ӧ�����Һ������أ�����ܷ�Ӧ�����ӷ���ʽΪ___________________________________��
��2����Al��NiO(OH)Ϊ�缫��NaOH��ҺΪ���Һ�������һ�����͵�أ��ŵ�ʱNiO(OH)ת��ΪNi(OH)2��
�ٸõ�صĸ�����Ӧʽ__________________���ڵ���ܷ�Ӧ�Ļ�ѧ����ʽ__________________��
��3��ij�������ƹ����п��ܺ���̼���ƺ��������ƣ��ֲⶨ�������Ƶĺ�����
��֪��5NaNO2+2KMnO4+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O
��ȡ4.000g���壬����ˮ���250mL��Һ��ȡ25.00mL��Һ����ƿ��,��0.1000mol��L������KMnO4��Һ���еζ���ʵ�������������±���ʾ��
����� | 1 | 2 | 3 | 4 |
KMnO4��Һ�����/ml | 20.60 | 20.02 | 20.00 | 19.98 |
�ٵ������һ������KMnO4��Һ����Һ___________��30���ڲ��ָ������жϴﵽ�ζ��յ㡣
�ڵ�һ��ʵ�����ݳ����쳣����������쳣��ԭ�������____________(�����)��
A����ʽ�ζ���������ˮϴ����δ�ñ�Һ��ϴ��
B����ƿϴ����δ���
C���ζ��������Ӷ���
�۸��ݱ������ݣ��������ù������������Ƶ���������_____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com