
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式:__________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为__________,其水溶液与F单质反应的化学方程式为____________________________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显______色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为______________;c的电子式为________;d的晶体类型是________。
(4)由A和B、D元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过________键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为__________。
(1)第一周期ⅠA族 2Cl-+2H2O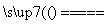 2OH-+H2↑+Cl2↑[或2NaCl(熔融)
2OH-+H2↑+Cl2↑[或2NaCl(熔融)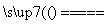 2Na+Cl2↑]
2Na+Cl2↑]
(2)纯碱(或苏打) Cl2+2Na2CO3+H2O===NaClO+NaCl+2NaHCO3 紫
(3)NaH Na2O2和Na2C2  金属晶体
金属晶体
(4)氢 正四面体
[解析] 根据题给信息,可推出A、B、D、E、F分别是H、C、O、Na、Cl。(1)工业上通常电解饱和食盐水制氯气,电解的离子方程式为2Cl-+2H2O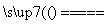 2OH-+H2↑+Cl2↑。(2)C、O、Na组成的盐中,Na的质量分数为43%的是Na2CO3,其俗名是纯碱(或苏打);首先写出化学方程式Cl2+H2O===HClO+HCl、HClO+Na2CO3===NaClO+NaHCO3、HCl+Na2CO3===NaCl+NaHCO3,然后将以上三个方程式合并得Cl2+2Na2CO3===NaClO+NaCl+2NaHCO3;产物中的NaClO具有强氧化性,能将I-氧化成I2,I2易溶于有机溶剂CCl4,I2的CCl4溶液呈紫色。(3)五种元素组成的物质中能形成阳离子的仅有Na,结合题给信息,可推知a是NaH、b是Na2O2、Na2C2;c为COCl2,其电子式为
2OH-+H2↑+Cl2↑。(2)C、O、Na组成的盐中,Na的质量分数为43%的是Na2CO3,其俗名是纯碱(或苏打);首先写出化学方程式Cl2+H2O===HClO+HCl、HClO+Na2CO3===NaClO+NaHCO3、HCl+Na2CO3===NaCl+NaHCO3,然后将以上三个方程式合并得Cl2+2Na2CO3===NaClO+NaCl+2NaHCO3;产物中的NaClO具有强氧化性,能将I-氧化成I2,I2易溶于有机溶剂CCl4,I2的CCl4溶液呈紫色。(3)五种元素组成的物质中能形成阳离子的仅有Na,结合题给信息,可推知a是NaH、b是Na2O2、Na2C2;c为COCl2,其电子式为 ;五种元素中只有Na形成的单质只存在一种类型的作用力且可导电,金属钠属于金属晶体。(4)H2O和CH4形成的可燃冰(CH4·nH2O)是一类新能源物质,其中H2O分子间形成氢键,CH4的空间构型为正四面体。
;五种元素中只有Na形成的单质只存在一种类型的作用力且可导电,金属钠属于金属晶体。(4)H2O和CH4形成的可燃冰(CH4·nH2O)是一类新能源物质,其中H2O分子间形成氢键,CH4的空间构型为正四面体。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列实验能获得成功的是( )
①甲烷气体通入空气中点燃获得热量
②甲烷气体通入氯水中制取一氯甲烷
③甲烷通入高锰酸钾酸性溶液,可使紫色褪去
④甲烷通入浓硝酸中分解得到碳单质和氢气
A.只有①② B.只有①
C.只有④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的说法错误的是( )
A.热稳定性:HCl>HI B.原子半径:Na>Mg
C.酸性: H2SO3>H2SO4 D.结合质子能力:S2->Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第________周期第________族;S的基态原子核外有________个未成对电子;Si的基态原子核外电子排布式为________________________。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si____S | O2-____Na+ | NaCl____Si | H2SO4____HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是________________________________________________________________________
________________________________________________________________________。
(4)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最外层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为________、__________、________。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有________、________。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是________。此化合物在酸性条件下与高锰酸钾反应的离子方程式为__________________________________________________;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图K162所示。下列说法不正确的是( )

图K162
A.离子半径的大小顺序为r(W2-)>r(Q-)>r(Y2-)>r(Z3+)
B.若存在简单阴离子R2-,则R不一定与Y、W同主族
C.元素X的氢化物与Q的氢化物化合的产物中既含有共价键又含有离子键
D.X、Z、W、Q四种元素的最高价氧化物对应的水化物均能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烷烃的混合物,在标准状况下其密度为1.03 g·L-1 ,则关于该混合物组
成的说法正确的是
A.一定有甲烷 B.一定有乙烷
C.不可能是甲烷和乙烷的混合物 D.可能是乙烷和丙烷的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
苯环结构中不存在C-C单键与C=C双键的交替结构,可以作为证据的是( )
①苯不能使溴水反应褪色
②苯不能使酸性高锰酸钾溶液褪色
③苯在一定条件下既能发生取代反应,又能发生加成反应
④经测定,邻二甲苯只有一种结构
⑤苯是正六边形
A.①②④⑤ B.①③④⑤ C.①②③④ D.②③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com