
����Ŀ����ͼ��ʾ��C��D��E��F��X��Y���Ƕ��Ե缫���ס�������Һ�������Ũ�ȶ���ͬ������ͨ��ǰ����Һ������䣩��A��BΪ���ֱ����Դ����������ֱ����Դ��ͨ����X����������ɫ��dz��Y����������ɫ�����ش� 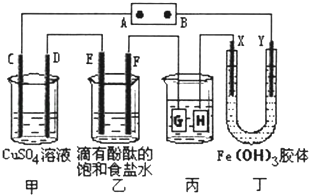
��1�����ס���װ���е�C��D��E��F�缫��ֻ��һ�ֵ�������ʱ����Ӧ���ʵ����ʵ���֮��Ϊ ��
��2�����ñ�װ�ø�ͭ����������������Һ��pH��13ʱ����ʱ����Һ���Ϊ500mL�������жƼ���������������Ϊ ��
��3��Fe��OH��3������Ʊ����ϸ��Ҫ��С������FeCl3��Һ�еμ�NaOH��Һ���Ʊ�Fe��OH��3���壬����ܿ�������˺��ɫ�ij������������Һ��pH=5�����ʱ��Һ��c��Fe3+��=mol/L������֪Ksp=1��10��36����
��4�����ü���ȼ�ϵ�أ��������ҺΪ2L2mol/LKOH��Һ���ṩ��Դ������ͨ����飬�ڱ�״���£����ļ�������VL��������CH4�������44.8��V��89.6ʱ����ʱ��Դ��B�������ĵ缫��ӦΪ�� ��
���𰸡�
��1��1��2��2��2
��2��5.4g
��3��10��9
��4��CH4��8e��+9CO32��+3H2O=10HCO3��
���������⣺��1��C��D��E��F�缫�����ĵ缫��Ӧ�ֱ�Ϊ��4OH���TO2��+2H2O+4e����Cu2++2e���TCu��2Cl���TCl2��+2e����2H++2e���TH2���������缫ת�Ƶ��Ӿ�Ϊ1molʱ�����ɵ��ʵ����ֱ�Ϊ��0.25mol��0.5mol��0.5mol��0.5mol�����Ե��ʵ����ʵ���֮��Ϊ1��2��2��2�����Դ��ǣ�1��2��2��2����2�����װ���У��Ʋ�����������������Ƽ�������������HӦ���ǶƼ������Һ���жƲ���������ӣ��ʵ��ҺΪAgNO3��Һ����������Һ��pH��13ʱ����Һ��c��OH����=0.1molL��1ʱ�����ݵ缫��Ӧ2H2O+2e���TH2��+2OH�� �� ��ŵ�������ӵ����ʵ���Ϊ��0.1mol/l��0.5L=0.05mol����ת��0.05mol����ʱ�����жƼ���������������=108g/mol��0.05mol=5.4g�����Դ��ǣ�5.4g����3��Fe��OH��3������Һ�У�c��H+��=10��5mol/L��Fe��OH��3Fe3++3OH�����ɵ���������c��OH����=10��9mol/L������Ksp=c��Fe3+��c��OH����3=1��10��36 �� ���c��Fe3+��=10��9mol/L�����Դ��ǣ�10��9����4��n��KOH��=2mol/L��2L=4mol����װ����ȼ�ϵ�أ������ϼ���ʧ���ӷ���������Ӧ�������������õ��ӷ�����ԭ��Ӧ��44.8L��V��89.6Lʱ������ԭ���غ��2mol��n��CO2����4mol����Ӧ����̼����أ�������ӦʽΪCH4��8e��+9CO32��+3H2O=10HCO3�� �� ���Դ��ǣ�CH4��8e��+9CO32��+3H2O=10HCO3�� ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������оٵ���ij���������ɺ����ʣ���˵�������ʿ϶����л�����ǣ� ��
A.����̼��������Ԫ�����
B.����̼���⡢������Ԫ�����
C.��������ȼ��ֻ���ɶ�����̼
D.�۵�Ͷ���������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����ʵ��������������״�ȼ�ϵ������Դ���������ͭ��Һ�� 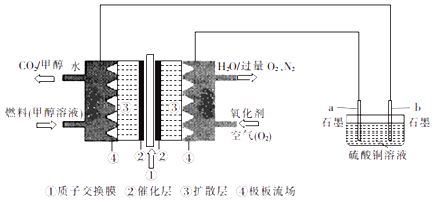
��ش��������⣺
��1��ͨ�������ĵ缫Ϊ�������������������ͨ��״�һ���ĵ缫��ӦʽΪ ��
��2��b�缫�ϵ�����Ϊ ��
��3����������ͭ��Һ�����Ϊ600mL�����ǰ����Һ������仯���Բ��ƣ���������336mL����״����O2 �� ���������ͭ��Һ��pHΪ ��
��4����a��b������ͭ�缫������һ��ʱ�������ͭ��Һ��Ũ�����������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ��������۵�674�桢�е�1023�棻���Ȼ�����300��������������������ˮ������ǿ�ҵ���ˮ�ԣ���500���������Ȼ��������������ܷ������ַ�Ӧ����Ӧ֮һΪ��12FeCl2+3O2 ![]() 2Fe2O3+8FeCl3 �� ij�о�С��ѡ������װ�ã��г�װ��ʡ�ԣ�װ�ÿ��ظ�ѡ�ã����з�Ӧ��̽�����ش��������⣺
2Fe2O3+8FeCl3 �� ij�о�С��ѡ������װ�ã��г�װ��ʡ�ԣ�װ�ÿ��ظ�ѡ�ã����з�Ӧ��̽�����ش��������⣺ 
��1��װ�õĺ�������˳��ΪA����D������Eװ��U�ι�������Ϊ�ֵ��ܵ�Ŀ���� ��
��2��Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3����Ӧ���̷��֣�װ��B�г����ɺ���ɫ�����⣬���۲쵽����ɫ���壬���ɸ�����Ļ�ѧ����ʽΪ ��
��4����B�г�ַ�Ӧ��ֹͣ���Ⱥ������ͨ������ ��
��5�����ʵ�飺 ������Eװ��U�ι���Ĺ�����֤Fe��OH��3����� ��
�ڲⶨװ��B�IJ�����������Ԫ�ص����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з��Ӿ����ڼ��Է���������ԭ�Ӿ�Ϊsp3�ӻ����ǣ� ��
A.CH4��P4
B.SO2��CHCl3
C.PCl3��SO3
D.NH3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ԭ����������ʾ������Ԫ�أ����γ�AB2�����ӻ�������ǣ� ��
A.6��8
B.11��13
C.11��16
D.12��17
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾһЩ�����е�ijЩ�ṹ����ش��������⣺ 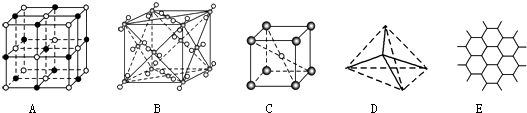
��1���������ʯ���ǣ�����ĸ��ţ���ͬ�� �� ����ÿ��̼ԭ������̼ԭ������Ҿ�����ȣ�
��2������ʯī���� �� ÿ����������ռ�е�̼ԭ����ƽ��Ϊ����
��3������NaCl���� �� ÿ��Na+��Χ��������Ҿ�����ȵ�Na+������
��4������CsCl���� �� ÿ��Cs+����Cl�����ڣ�
��5�������ɱ����� �� ÿ��CO2��������CO2���ӽ��ڣ�
��6����֪ʯī��̼̼���ļ����Ƚ��ʯ��̼̼���ļ����̣����������������۵��ɸߵ��͵�����˳��Ϊ������ĸ��Żش𣩣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaNO2����һ�־�����ζ���ж����Ҽ۸��ʳ�Σ�NaCl�����˵Ĺ�ҵ���Σ���������ʳ��ʹ�ã����¶����ж��¹ʷ��������IJ������ʼ���ͼ������˵��������ǣ� �� 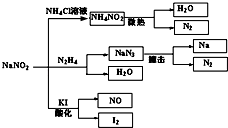
A.��ͼ���漰���Ļ�ѧ��Ӧ����������ԭ��Ӧ
B.N2H4��������ˮ����Ϊ���Ǽ��Է�������ˮ����֮�����γ����
C.NaNO2��N2H4����NaN3�ķ�Ӧ����ʽΪ��NaNO2+N2H4=NaN3+2H2O
D.���õ��۵⻯����ֽ��ʳ����ʳ�Σ�NaCl�����������ƣ�NaNO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧ����������Ϊ���������Ϳ�ű���������أ����2015��ŵ�������������ؿ�����éȩΪԭ����ȡ������˵��������ǣ� �� 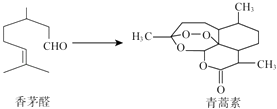
A.��éȩ��ʹBr2��CCl4��Һ��ɫ
B.�����ط���ʽΪC15H22O5
C.�����غ��к�H2O2��ͬ�Ĺ�����
D.�������������������ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com