
 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.分析 (1)依据热化学方程式 和盖斯定律计算得到;
(2)根据盖斯定律计算水分解反应的焓变,化学反应的焓变△H=H产物-H反应物再结合化学键能和物质能量的关系来回答;
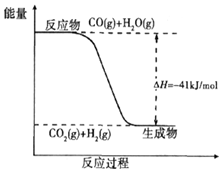
(3)依据图象分析反应物能量高于生成物能量,反应是放热反应,依据反应的热化学方程式标注物质聚集状态和对应焓变的大小.
解答 解:(1)①C(s)+$\frac{1}{2}$O2(g)=CO(g)△H1=-110.5kJ/mol
②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ/mol
依据盖斯定律①-$\frac{②}{2}$得到:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3KJ/mol;
故答案为:+131.3;
(2)已知①:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3KJ/mol,
②C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1=-110.5kJ•mol-1
①×2-②×2得:2H2O(g)═O2(g)+2H2(g)△H=(2×131.3KJ+221)kJ•mol-1,
4×m-496-2×436=2×131.3KJ+221,
解得m=+462.9,故答案为:462.9;
(3)图象分析判断反应物能量高于生成物能量,反应是放热反应,1molCO完全反应放出的热量41KJ,热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41 kJ/mol;
故答案为:放热;CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41 kJ/mol.
点评 本题考查热化学方程式的书写和盖斯定律应用,图象分析理解是关键,题目较简单.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在合成氨工业中,加压有利于提高NH3的产率 | |
| B. | 直接燃烧煤不如将煤进行深加工后再燃烧的效率好 | |
| C. | 化石燃料包括石油、天然气、煤和氢能 | |
| D. | 在时间允许的情况下,从节能上分析,步行>坐公交>坐出租车 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入水时,平衡向逆反应方向移动 | |
| B. | 加入少量CH3COONa固体,平衡向逆反应方向移动,c(CH3COO-)增大 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量NaOH固体,平衡向正反应方向移动,酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com