
A.2SO2+O2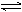 2SO3; △H=-196.6kJ/mol 2SO3; △H=-196.6kJ/mol |
| B.C(s)+O2(g)==CO2(g);△H=393.5kJ/mol |
| C.1/2H2(g)+1/2Cl2(g)==HCl(g);△H=-92.5kJ/mol |
| D.H+(aq)+OH-(aq)==H2O(l);△H=57.3kJ |
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源:不详 题型:填空题
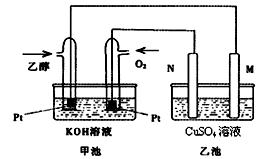
 下),理论上需通入乙醇 g?
下),理论上需通入乙醇 g?查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
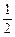 O2(g)=CO2(g) ΔH3<0 ③
O2(g)=CO2(g) ΔH3<0 ③ 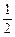 O2(g)=H2O(g) ΔH4<0 ④
O2(g)=H2O(g) ΔH4<0 ④查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 ,中和后生成溶液的比热容为C J/(g.℃)反应前的温度为18℃,反应后最高温度为t℃,则中和热的计算式是△H=________________________。
,中和后生成溶液的比热容为C J/(g.℃)反应前的温度为18℃,反应后最高温度为t℃,则中和热的计算式是△H=________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
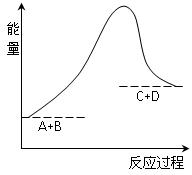
 C(g) +D(g)过程中的能量变化如图所示,则下列说法正确的是
C(g) +D(g)过程中的能量变化如图所示,则下列说法正确的是
| A.该反应是放热反应 |
| B.反应体系中加入催化剂对反应热有影响 |
| C.当反应达到平衡时,升高温度,A的转化率减小 |
| D.改变压强与加催化剂对反应的影响原因相同,都不会使平衡发生移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.焓变为正值的反应都是吸热反应 |
| B.放热的熵增加反应一定能自发进行 |
| C.同一条件下,氨水在物质的量浓度不同的溶液中,其电离程度是不相同的 |
| D.强电解质都是离子化合物,弱电解质都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 中和热为57.3kJ/mol 。下列热化学方程式正确的是
中和热为57.3kJ/mol 。下列热化学方程式正确的是| A.HNO3(aq)+KOH(aq)=H2O(l) +KNO3(aq)ΔH > -57.3kJ/mol. |
B.HNO3(aq)+NH3 ·H2O(aq)=H2O(l) +KNO3(aq)ΔH <  -57.3kJ/mol. -57.3kJ/mol. |
| C.CH3COOH(aq)+KOH(aq)=H2O(l) + CH3COOK(aq) ΔH< -57.3kJ/mol. |
| D.CH3COOH(aq)+ NH3 ·H2O(aq)=H2O(l) + CH3COONH4(aq) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应为放热反应 | B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 | D.该反应只有在加热条件下才能进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com