
分析 (1)先根据溶液质量及氯化铜的质量分数计算出氯化铜的质量,然后根据n=$\frac{m}{M}$计算出该溶液中氯化铜的物质的量,然再根据c=$\frac{n}{V}$计算出此溶液中CuCl2的物质的量;
(2)溶液具有均一性,取出溶液浓度不变,然后结合稀释过程中溶质的物质的量不变计算出稀释后氯化铜溶液的浓度.
解答 解:(1)270g质量分数为10%的CuCl2溶液中含有氯化铜的质量为:270g×10%=27g,该氯化铜的物质的量为:$\frac{27g}{135g/mol}$=0.2mol,
则该溶液中CuCl2的物质的量为:c(CuCl2)=$\frac{0.2mol}{0.1L}$=2mol/L,
答:此溶液中CuCl2的物质的量为2mol/L;
(2)从上述溶液中取出10mL加水稀释成100mL,取出溶液浓度为2mol/L,稀释过程中氯化铜的物质的量不变,则稀释后溶液中CuCl2溶液的物质的量浓度是:$\frac{2mol/L×0.01L}{0.1L}$=0.2mol/L,
答:稀释后所得的CuCl2溶液的物质的量浓度为0.2mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量与摩尔质量、物质的量浓度之间的关系为解答关键,注意掌握溶质质量分数的概念及应用,试题侧重考查学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
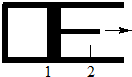 一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g).达平衡后,测得A的浓度为0.5mol•L-1.恒温下将活塞由1处拉到2处,再次达到平衡后,测得A的浓度为0.225mol•L-1.则下列说法中,正确的是( )
一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g).达平衡后,测得A的浓度为0.5mol•L-1.恒温下将活塞由1处拉到2处,再次达到平衡后,测得A的浓度为0.225mol•L-1.则下列说法中,正确的是( )| A. | x+y<z | B. | 平衡向逆反应方向移动 | ||
| C. | B的转化率减小 | D. | C的体积分数降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HAt很稳定 | |
| B. | 砹单质易溶于水难溶于某些有机溶剂 | |
| C. | AgAt不溶于水 | |
| D. | 砹单质(At2)氧化性很强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 交警检查司机是否酒后驾车的原理中体现了乙醇的氧化性 | |
| B. | 硅胶多孔,吸附水分能力强,常用作袋装食品、瓶装药品的干燥剂 | |
| C. | 铜的金属活动性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 | |
| D. | 以石油、煤和天然气为原料通过聚合反应可以获得用途广泛的高分子合成材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
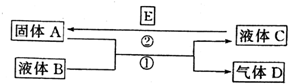 中学化学中有很多物质可以实现图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物.
中学化学中有很多物质可以实现图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl(Na2CO3) | B. | Fe(Cu) | C. | Na2CO3(CaCO3) | D. | HCl(BaCl2) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
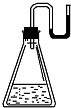 有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com