
| 反应阶段 | I | II | III |
| 盐酸体积x/mL | 0<x≤10.0 | 10.0<x≤40.0 | x>40.0 |
| 现 象 | 无气体 | 产生气体 | 无气体 |
| 解释 | CO32-+H+=HCO3- |
分析 (1)根据c=$\frac{1000ρω}{M}$计算出浓盐酸的物质的量浓度,再根据溶液稀释过程中溶质的物质的量不变计算出需要浓盐酸的体积;根据配制1.0mol•L-1的稀盐酸250mL的步骤选用仪器,然后判断还缺少的仪器;
(2)第Ⅰ阶段无气体生成说明盐酸滴入溶液中发生的是碳酸根离子和氢离子生成碳酸氢根离子的过程,反应生成的碳酸氢根离子与氯化氢的物质的量相等;第Ⅱ阶段碳酸氢根离子与氢离子反应生成二氧化碳气体;根据盐酸中氯化氢的物质的量可计算出碳酸根离子的物质的量,再根据c=$\frac{n}{V}$计算出原混合液中碳酸根离子的浓度.
解答 解:(1)36.5%的浓盐酸的密度约为1.2g•cm-3的浓盐酸的物质的量浓度为:$\frac{1000×1.2×36.5%}{36.5}$mol/L=12.0mol/L,
配制250mL 1.0mol/L的稀盐酸需要该浓盐酸的体积为:$\frac{1.0mol/L×0.25L}{12.0mol/L}$≈0.0208L=20.8mL;
根据配制250mL 1.0mol/L的稀硫酸步骤可知,需要选用的仪器为:量筒、烧杯、玻璃棒、250mL容量瓶、胶头滴管,所以还缺少的仪器为:250mL容量瓶、胶头滴管,
故答案为:20.8;250mL容量瓶、胶头滴管;
(2)第一阶段无气体生成说明盐酸滴入溶液中发生的是碳酸根离子和氢离子生成碳酸氢根离子的过程,反应为CO32-+H+=HCO3-,消耗盐酸体积10mL,碳酸钠全部转化为碳酸氢钠,氯化氢物质的量为:0.010L×1.00mol•L-1=0.01mol,c(CO32-)=$\frac{0.01mol}{0.02L}$=0.500mol/L;
第二阶段生成二氧化碳气体,发生反应为:HCO3-+H+=H2O+CO2↑,
故答案为:HCO3-+H+=H2O+CO2↑;0.500 mol•L-1.
点评 本题考查了物质的量浓度的计算、混合物反应的计算,题目难度中等,注意掌握配制一定浓度的溶液方法,(2)为易错点,明确发生反应的实质为解答关键,试题培养了学生的化学实验、化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
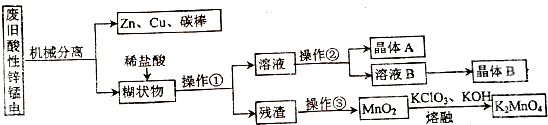
 酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、NH4Cl等组成的糊状填充物,其结构如下图.该电池在放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH
酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、NH4Cl等组成的糊状填充物,其结构如下图.该电池在放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH| 温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应的离子方程式:2H++CO32-═H2O+CO2↑ | |
| B. | 若向Na2CO3溶液中通入足量的SO2气体,也可得到CO2 | |
| C. | HSO3-的水解程度大于其电离程度 | |
| D. | 各级电离常数:K1(H2SO3)>K1(H2CO3)>K2(H2SO3)>K2(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁铝合金的抗腐蚀能力强,不与稀硫酸反应 | |
| B. | Na的金属活动性比Mg的强,故可用Na与MgCl2溶液反应制Mg | |
| C. | 钠可与冷水剧烈反应,而镁与热水才能反应,说明钠比镁活泼 | |
| D. | Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中,Fe也显+3价 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH为2的醋酸溶液与pH为12的氢氧化钠溶液 | |
| B. | 0.0l mol•L-1 的醋酸溶液与0.01 mol•L-1的氢氧化钠溶液 | |
| C. | pH为2的硫酸溶液与pH为12的氢氧化钠溶液 | |
| D. | 0.010 mol•L-1的盐酸溶液与0.010 mol•L-1的氢氧化钡溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.4gH2O2含有极性键的数目为0.2NA | |
| B. | 1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA | |
| C. | 电解精炼铜时,若转移了NA个电子,则阳极质量减小32g | |
| D. | 标况下,11.2LSO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 现象或反应事实 | 解释 |
| A | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝的熔点比铝高 |
| B | 工业合成氨反应需在高温条件下进行 | 提高氨的产率 |
| C | 镀层破损后,镀锡的铁比镀锌的铁易腐蚀 | 锡比锌活泼 |
| D | 2CO═2C+O2在任何条件下均不能自发进行 | 该反应△H>0,△S<0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com