
| A.加入适量镁粉 | B.加入适量的水 |
| C.加入几滴硫酸铜溶液 | D.再加入少量稀硫酸 |
科目:高中化学 来源:不详 题型:单选题
| A.改变正、逆反应速率,但改变的程度不同 |
| B.提高反应物达到平衡时的转化率 |
| C.缩短到达平衡所用的时间 |
| D.提高生成物在平衡体系中的质量分数 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.其它条件不变时,升高温度化学反应速率加快 |
| B.其它条件不变时,增大浓度化学反应速率加快 |
| C.化学反应达到反应限度时,正反应速率和逆反应速率相等 |
| D.化学反应达到反应限度时,反应物的浓度和生成物的浓度相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.①③ | C.①② | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开始时的反应速率:V(锌粒)>V(锌粉) |
| B.溶液温度升高的快慢:T(锌粒)>T(锌粉) |
| C.最后放出H2的总量:n(锌粒)>n(锌粉) |
| D.达平衡时正逆反应的速率相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
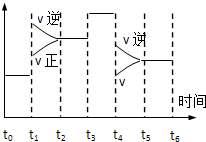
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增加水的量或温度,可以加快镁跟水的反应速率 |
| B.硫酸的浓度越大,锌与硫酸反应制取氢气的速率就越大 |
| C.对反应3H2(g)+N2(g)?2NH3(g),在密闭容器中进行(固定体积),若充入氦气,则压强增大,化学反应速率加快 |
| D.对反应3H2(g)+N2(g)?2NH3(g),使用催化剂,正逆反应速率同等程度加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com