
电渗析法是一种利用离子交换膜进行海水淡化的方法,工作原理如图。下列有关说法错误的是
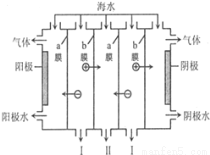
A.阳极可发生电极反应:2Cl--2e-═Cl2↑
B.阴极附近溶液的pH减小
C.a膜为阴离子交换膜,b膜为阳离子交换膜
D.I、II分别是淡水、浓海水出口
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:2015-2016学年新疆石河子二中高二下期末化学试卷(解析版) 题型:选择题
某有机物的结构简式如图所示。Na、NaOH、NaHCO3分别与等物质的量的该物质恰好反应时,Na、NaOH、NaHCO3的物质的量之比为( )
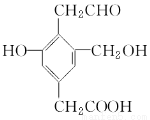
A.3∶3∶2
B.3∶2∶1
C.1∶1∶1
D.3∶2∶2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高二下期末化学试卷(解析版) 题型:填空题
目前,消除氮氧化物污染有多种方法。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4 (g)+4NO2 (g)=4NO(g)+CO2 (g)+2H2 O(g) ΔH=-574 kJ·mol-1
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2 O(g) ΔH=-1160 kJ·mol-1
③H2O(g)=H2O(l) ΔH=-44.0 kJ·mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l)的热化学方程式________
(2)用活性炭还原法处理氮氧化物。有关反应为:C(s)+2NO(g) 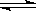 N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
N2 (g)+CO2 (g)某研究小组向恒容密闭容器加入一定量的活性炭NO,恒温条件下反应,反应进行到不同时间测得各物质的浓度如下
浓度/mol·L-1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①不能作为判断反应达到化学平衡状态的依据是_____ __
A.容器内CO2的浓度保持不变
B.v正(N2)=2 v正(NO)
C.容器内压强保持不变
D.混合气体的密度保持不变
E.混合气体的平均相对分子质量保持不变
②在该温度下时.该反应的平衡常数为 (保留两位小数);
③在30 min,改变某一条件,反应重新达到平衡,则改变的条件是___ __。
(3)合成塔失去活性的铬锌触媒可用于制备锌锰电池。在碱性条件下,该电池的总反应为:Zn(s)+2MnO2 (s)+H2O(l)= Zn(OH)2 (s)+Mn2O3(s),该电池正极的电极反应式是 。PbO2 可以通过石墨为电极,Pb(NO3)2和Cu(NO3)2的混合溶液为电解液电解制取。阳极发生反应的电极反应式为 ,阴极上观察到的现象是 ;若电解液中不加入Cu(NO3)2这样做的主要缺点是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省华蓥市高二下期末化学试卷(解析版) 题型:选择题
常温下下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO3-、K+
C.c(H+)/c(OH-)=1×1012的溶液中:NH4+、Cl-、NO3-、Al3+
D.c(Fe3+)=0.1 mol/L的溶液中:K+、ClO-、SO42—、SCN-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:填空题
下表为长式周期表的一部分,其中的编号代表对应的元素。
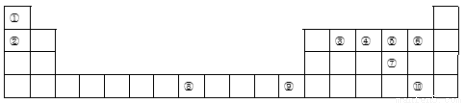
(1)比较①和②具有相同核外电子排布的简单离子半径大小关系为______________(填化学式);③、④、⑤三种元素的第一电离能由大到小的顺序为____________(填元素符号),写出原子序数和元素⑧相差2且元素⑧同族的元素基态原子的外围电子排布式____________。
(2)在元素③与①形成的原子个数比为1:1的四原子分子中,③原子的杂化方式为____________。其分子中δ键和π键数目之比为____________。
(3)元素④的某种氢化物甲分子中含有18个电子,甲为二元弱碱,在水中的电离方程式与氨相似。写出甲在水中的第一步电离的电离方程式____________。甲在微电子工业中,可作刻蚀剂H2O2的清除剂,二者发生反应的产物不污染环境,其化学方程式为____________。
(4)元素⑥和⑤形成分子乙的结构与元素①和⑤形成的最简单分子丙相似,乙的VSEPR模型为___________,解释丙的沸点高于乙的原因____________。
(5)可用赤血盐K3[Fe(CN)6]检验元素⑧的+2价阳离子,写出该反应的离子方程式___________,元素⑩的阴离子与元素⑧的+2价离子形成化合物丁,将3molCl2通入含4mol丁的溶液,用一个离子方程式表示该反应过程为____________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为⑦和⑨组成的离子化合物戊的晶胞,其中三个离子(白色球)坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D离子(黑色球)的坐标参数为_____。
,0)。则D离子(黑色球)的坐标参数为_____。
②晶胞参数,描述晶胞的大小和形状,已知戊的晶胞参数apm,则晶胞中B和D离子的距离为______pm。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述不正确的是
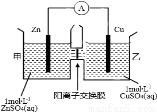
A.Zn电极上发生氧化反应
B.电子的流向为Zn→电流表→Cu
C.SO42-由乙池通过离子交换膜向甲池移动
D.电池工作一段时间后,乙池溶液的总质量明显增加
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二下期末化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0,下列叙述正确的是
4NO(g)+6H2O(g) △H<0,下列叙述正确的是
A.达到化学平衡时4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.达到化学平衡时,若升高温度,则正反应速率减小,逆反应速率增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古高一下期末化学试卷(解析版) 题型:选择题
在相同温度时100mL0.01mol/L的醋酸溶液与10mL0.1mol/L的醋酸溶液相比较,下列数值前者大于后者的是( )
A.中和时所需NaOH的量
B.电离程度
C.H+的物质的浓度
D.CH3COOH的物质的量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二下期末化学试卷(解析版) 题型:选择题
每年的6月26日是国际禁毒日,珍爱生命,远离毒品。以下是四种毒品的结构简式,下列有关说法正确的是
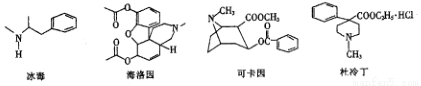
A.冰毒的摩尔质量为149
B.海洛因和杜冷丁均能与溴水发生加成反应
C.1mol可卡因最多能与2molNaOH发生反应
D.以上毒品均属于芳香烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com