

| A. | 最高正化合价:Z>X | |
| B. | X、Y、Z的单质中,Z单质的熔点最高 | |
| C. | 若X为非金属元素,则离子半径:Xn->Ym->Zm- | |
| D. | X最高价氧化物对应的水化物,要么是强酸,要么是强碱 |
分析 短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示,则Z为第二周期元素,X、Y为第三周期元素,
A.Z可能为O或F;
B.Z、Y若均在ⅤⅡA,单质的相对分子质量大的熔点高,且X可能为Si;
C.若X为非金属元素,X、Y的离子具有相同电子层结构,原子序数大的离子半径小;
D.由位置可知,X可能是Al,也可能是Si.
解答 解:短周期主族元素X、Y、Z在元素周期表中的相对位置如图所示,则Z为第二周期元素,X、Y为第三周期元素,
A.Z可能为O或F,则Z没有最高正价,故A错误;
B.Z、Y若均在ⅤⅡA,单质的相对分子质量大的熔点高,且X可能为Si,则可能X的熔点最高,故B错误;
C.若X为非金属元素,X、Y的离子具有相同电子层结构,原子序数大的离子半径小,则离子半径:Xn->Ym->Zm-,故C正确;
D.由位置可知,X可能是Al,也可能是Si,则最高价氧化物对应水化物有可能是两性氢氧化物或弱酸,故D错误;
故选:C.
点评 本题考查位置、结构与性质的关系,为高频考点,把握位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 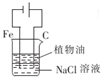 用图装置制取Fe(OH)2沉淀 | B. | 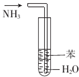 用图装置吸收NH3并防止倒吸 | ||
| C. | 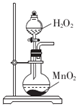 用图装置制取少量氧气 | D. | 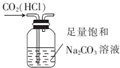 用图装置除去CO2中含有的少量HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
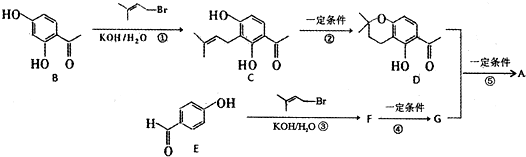
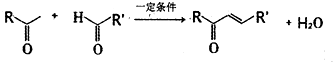
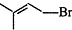 生成高分子化合物的方程式
生成高分子化合物的方程式 .
. 、
、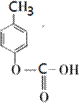 .
.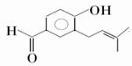 .
.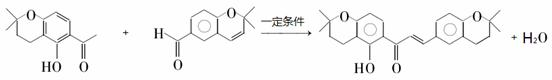 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
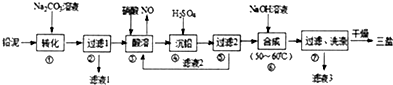
| A. | 步級①PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42- | |
| B. | 步骤③酸溶时,PbO、Pb、PbCO3都与硝酸反应生成Pb(NO3)2; 滤液2中可回收再利用的主要成分为HNO3 | |
| C. | 滤液1、滤液3中所含的溶质完全相同 | |
| D. | 步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH=3Na2SO4+3PbO•PbSO4•H2O+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入.硫磺可用于生产化工原料硫酸.某工厂用如图所示的工艺流程生产硫酸:
印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入.硫磺可用于生产化工原料硫酸.某工厂用如图所示的工艺流程生产硫酸:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在燃煤中加入适量的生石灰能有效减少二氧化硫的排放 | |
| B. | 控制含磷洗涤剂的生产和使用有利于防止水体富营养化 | |
| C. | 采用汽车尾气处理技术可将汽车尾气中的NO和CO转化为无害气体 | |
| D. | 使用加酶洗衣粉,水温越高,洗涤效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
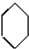 $→_{①}^{Cl_{2},光照}$
$→_{①}^{Cl_{2},光照}$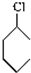 $→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$
$→_{△②}^{NaOH醇溶液}$A$→_{③}^{Cl_{2},不见光}$B$\stackrel{④}{→}$ $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$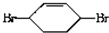 $\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$
$\stackrel{⑥}{→}$$→_{H_{2}}^{⑦}$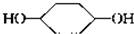
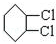 ,C
,C
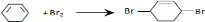 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与P4的分子结构都是正四面体形,因此在6.02×1023个CH4分子或P4分子中都含有4×6.02×1023个共价键 | |
| B. | 在含6.02×1023个硅原子的二氧化硅晶体中含有4×6.02×1023个Si-O键 | |
| C. | 28g CO、C2H4混合气体的分子总数NA,体积约为22.4L | |
| D. | 6.02×1023个Fe3+完全水解可以得到6.02×1023个氢氧化铁胶体粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
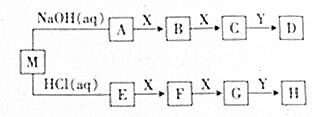 几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.
几种中学常见的短周期元素组成几种物质,它们的转化关系如图所示(部分条件和产物省略).已知M是酸式盐,只有X是单质,B、C、F、G、Y都是氧化物,D和H是两种常用的强酸.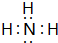 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com