
 (1)该反应的化学方程式为2N2O5?4NO2+O2
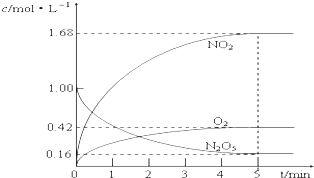
(1)该反应的化学方程式为2N2O5?4NO2+O2分析 (1)根据图中的有关物质的浓度的变化可以判断反应物、生成物,及它们之间量的关系,进而写出化学方程式;
(2)根据$\frac{△c}{△t}$求速率;
(3)根据影响速率的因素可判断,浓度越大反应速率越快;
(4)反应物为N2O5,转化率=$\frac{消耗量}{起始量}$×100%.
解答 (1)由图象可知,在5min时,NO2的浓度增加了1.68mol/L,O2的浓度增加了0.42mol/L,N2O5的浓度减小了1-0.16=0.84mol/L,所以NO2、O2为生成物,N2O5为反应物,它们的变化的浓度之比=1.68:0.42:0.84=4:1:2,所以化学反应方程式为:2N2O5?4NO2+O2,
故答案为:2N2O5?4NO2+O2;
(2)v (NO2)=$\frac{△c}{△t}$=$\frac{1.68mol/L}{5min}$=0.336mol/(L•min),故答案为:0.336mol/(L•min);
(3)因为在0~2 min内反应物平均浓度要比2~4min内的反应物浓度要大,浓度越大反应速率越快,
故答案为:0~2 min内c (N2O5)大于2~4min内的c(N2O5);
(4)该反应达到化学平衡状态时,反应物的转化率=$\frac{1mol/L-0.16mol/L}{1mol/L}$×100%=84%,
故答案为:84%.
点评 本题考查了学生运用图象写方程式由此求得反应速率、判断影响速率的因素的能力,题目难度不大.关键是要注意图中的物理量的理解应用.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
 原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期.
原子序数依次增大的A、B、C、D、E、F六种元素.其中A的基态原子有3个不同能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E、F和C位于同一主族,F处于第一个长周期.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将NaOH放在天平左边托盘中的纸片上 | |
| B. | 将NaOH放入烧杯中(烧杯事先已称重),并放在天平左边托盘上 | |
| C. | 用镊子取出标定为10.1 g的砝码放在天平右边的托盘上 | |
| D. | 用镊子取出标定为10 g的砝码放在天平左边的托盘上,并将游码向右移到0.1 g位置上 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.
Ⅰ:A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等.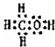 .
.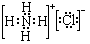 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
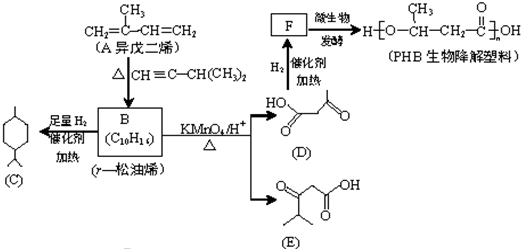
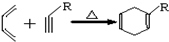 ,
,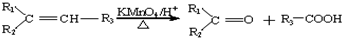 .
. .
.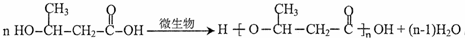 .
.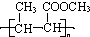 (一种类似有机玻璃的塑料).
(一种类似有机玻璃的塑料).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
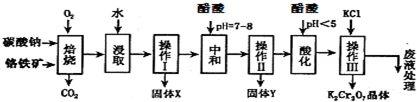
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度(g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com