
(9��)ijУһ��ѧʵ��С��ͨ��ʵ�������ȷ��һ��ɫ��ĩΪFe2O3��Cu2O�Ļ���
��֪:��Cu2O����ϡ��������Cu��CuSO4,��Cu2O�ڿ����м�������CuO��
(1)ʵ��С�����ü��ȷ��ⶨCu2O������������ȡa g�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊb g(b>a)����������Cu2O����������Ϊ__________��
(2)ʵ��С�������øú�ɫ��ĩ��ȡ�ϴ����ĵ���(CuSO4��5H2O)�����������ϵ�֪������Һ��ͨ��������Һ������Զ�ʹCu2����Fe2����Fe3���ֱ����ɳ�����pH���£�
|
|
�������↑ʼ����ʱ��pH |
�������������ȫʱ��pH |
��ѡ���Լ� |
|
Fe3+ |
1.9 |
3.7 |
A.��ˮ�� B.H2O2�� C.NaOH�� D.��ˮ�� E.CuO�� F.Cu2(OH)2CO3 |
|
Fe2+ |
7.5 |
11 |
|
|
Cu2+ |
6.0 |
10 |
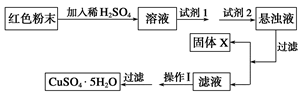
ʵ��С���������ͼʵ�鷽����
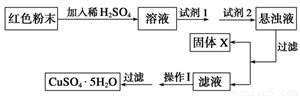
�Իش�
���Լ�1����Ϊ________________���Լ�2����Ϊ________________��
�ڹ���X�Ļ�ѧʽΪ____________��
�۲�����Ϊ____________________��
(1)��100%��3�֣�
(2)��B;��1�֣� EF����2�֣� ��Fe(OH)3��1�֣� ������Ũ������ȴ�ᾧ��2�֣�
����������1��������ͭ��������ͭ�ķ���ʽΪ2Cu2O��O2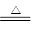 4CuO�����Ը��ݲ�������֪��������ͭ��������
4CuO�����Ը��ݲ�������֪��������ͭ��������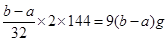 �����Ի������Cu2O����������Ϊ��100%��
�����Ի������Cu2O����������Ϊ��100%��
��2���ٻ������Һϡ�����У���������ͭ��ͭ��������������Ӧ�ü���˫��ˮ��������ͭ�����Լ�1��B���Լ�2��ԭ��������ҺpHֵ�ģ����ڲ����������ʣ����Է�Ӧ��EF��
��ͨ������pH������������������������X��Fe(OH)3��
��Ҫ�õ�����ͭ���壬Ӧ��ͨ������Ũ������ȴ�ᾧ�������˵õ���


 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д� �����ܾ�ϵ�д�
�����ܾ�ϵ�д� ���ƿ�����ϵ�д�
���ƿ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 9(b-a) |
| a |
| 9(b-a) |
| a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 9(b-a) |
| a |
| 9(b-a) |
| a |
| ���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
| ��ʼ����pH | 6.0 | 7.5 | 1.4 |
| ������ȫpH | 13 | 14 | 3.7 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
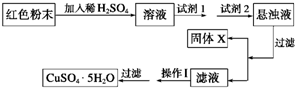 ijУһ��ѧʵ��С��ͨ��ʵ�������ȷ��һ��ɫ��ĩΪFe2O3��Cu2O�Ļ���
ijУһ��ѧʵ��С��ͨ��ʵ�������ȷ��һ��ɫ��ĩΪFe2O3��Cu2O�Ļ���| 100(b-a) |
| a |
| 100(b-a) |
| a |
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | ��ѡ���Լ� | |
| Fe3+ | 1.9 | 3.7 | A����ˮ��B��H2O2�� C��NaOH��D����ˮ�� E��CuO��F��Cu2��OH��2CO3 |
| Fe2+ | 7.5 | 11 | |
| Cu2+ | 6.0 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ�ϲ����и�����һ�ο��Ի�ѧ�Ծ����������� ���ͣ�ʵ����
(9��)ijУһ��ѧʵ��С��ͨ��ʵ�������ȷ��һ��ɫ��ĩΪFe2O3��Cu2O�Ļ���
��֪:��Cu2O����ϡ��������Cu��CuSO4,��Cu2O�ڿ����м�������CuO��
(1)ʵ��С�����ü��ȷ��ⶨCu2O������������ȡa g�����ĩ�ڿ����г�ּ��ȣ����������ٱ仯ʱ����������Ϊb g(b>a)����������Cu2O����������Ϊ__________��
(2)ʵ��С�������øú�ɫ��ĩ��ȡ�ϴ����ĵ���(CuSO4��5H2O)�����������ϵ�֪������Һ��ͨ��������Һ������Զ�ʹCu2����Fe2����Fe3���ֱ����ɳ�����pH���£�
| | �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | ��ѡ���Լ� |
| Fe3+ | 1.9 | 3.7 | A.��ˮ�� B.H2O2�� C.NaOH�� D.��ˮ�� E.CuO�� F.Cu2(OH)2CO3 |
| Fe2+ | 7.5 | 11 | |
| Cu2+ | 6.0 | 10 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com