
分析 根据c=$\frac{1000ρω}{M}$计算37%,密度为1.19g/ml该浓盐酸的物质的量浓度;根据稀释定律:稀释前后HCl的物质的量相等计算需要浓盐酸的体积.根据m=ρv计算需加水多少克.
解答 解:根据c=$\frac{1000ρω}{M}$可知,该浓盐酸的物质的量浓度为$\frac{1000×1.19×37%}{36.5}$mol/L≈12mol/L,设需要浓盐酸的体积为V,根据稀释定律,稀释前后HCl的物质的量相等,则:V×12mol/L=250mL×1mol/L,解得V≈20.83mL,250毫升,密度为1.1g/ml,1mol/L的稀盐酸溶液的质量为m=ρv=1.1g/ml×250毫升=275g,37%,密度为1.19g/ml的浓盐酸20.83mL的质量为m=ρv=1.19g/ml×20.83mL≈25g,需加水275g-25g=250g,水的密度为1g/cm3,所以需加水250克(毫升),
答:需用37%,密度为1.19g/ml的浓盐酸20.83mL;需加水250克(毫升).
点评 本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数计算,注意理解掌握物质的量浓度与质量分数之间的关系是解答关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3 | B. | NH4Cl | C. | NH4NO3 | D. | (NH4)2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盖斯定律为我们提供了解决很难由实验直接测定而获得反应热的理论依据 | |
| B. | 若用50mL 0.50mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.25mo1•L-1的硫酸充分反应,两反应测定的反应热不相等 | |
| C. | 实验时只需要记录反应体系的最高温度t即可 | |
| D. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,再用环形玻璃搅拌棒不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-的结构示意图: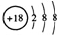 | |
| B. | 质子数为53,中子数为78的碘原子:${\;}_{53}^{131}$I | |
| C. | 光导纤维主要成分的化学式:Si | |
| D. | H216O、D216O、H218O、D218O互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
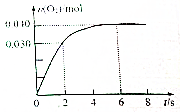 一定温度下,向2.0L恒容密闭容器中充入0.88mol NO2(g),发生反应:2NO2(g)?O2(g)+2NO(g),得到O2的物质的量随时间变化曲线如图所示,回答下列问题:
一定温度下,向2.0L恒容密闭容器中充入0.88mol NO2(g),发生反应:2NO2(g)?O2(g)+2NO(g),得到O2的物质的量随时间变化曲线如图所示,回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com