
人工合成化合物NH5 可改写成HN4H,能和水反应:NH5 + H2O==NH3.H2O + H2↑.下列说法正确的是( )
A. NH5属于离子化合物,该反应中水做氧化剂
B.该反应属于氧化还原反应,NH5既是氧化剂又是还原剂
C.该反应不属于氧化还原反应,属于复分解反应
D.标准状况下每生成22.4LH2时,转移2NA电子
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:
下列有关说法中正确的是
①12C和14C的化学性质相同 ②37Cl原子核内中子数为17 ③12CO2和14CO2互为同位素 ④Ca和Ca2+是同种元素,且性质相同 ⑤37Cl-的结构示意图为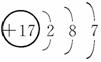
A.②③ B.③④
C.①④⑤ D.①
查看答案和解析>>
科目:高中化学 来源: 题型:
铜制品上的铝质铆钉,在潮湿空气中易被腐蚀的原因是( )
A.形成原电池时铝作负极 B.形成原电池时铜作负极
C.形成原电池时,电流由铝经导线流向铜 D.铝质铆钉被空气中的氧气氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
我国首创以铝—空气—海水电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使铝不断氧化而产生电流。只要把灯放入海水中数分钟,就会发生耀眼的白光。则该电源负极材料为____________,正极材料为____________,正、负极反应分别是________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐)。实验室以盐泥为原料制取MgSO4·7H2O的实验过程如下:

 已知:①室温下Ksp[Mg(OH)2]=6.0×10-12。②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7。③三种化合物的溶解度(S)随温度变化的曲线如图所示。
已知:①室温下Ksp[Mg(OH)2]=6.0×10-12。②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7。③三种化合物的溶解度(S)随温度变化的曲线如图所示。
(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是______________________。
(2)若室温下的溶液中Mg2+的浓度为6.0 mol·L-1,则溶液pH≥________才可能产生Mg(OH)2沉淀。
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是__________________,滤渣的主要成分是______________________。
(4)从滤液Ⅱ中获得MgSO4·7H2O晶体的实验步骤依次为①向滤液Ⅱ中加入______________;②过滤,得沉淀;③________________;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品。
(5)若获得的MgSO4·7H2O的质量为24.6 g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为________(MgSO4·7H2O的相对分子质量为246)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A.(2013·安徽)HCHO分子中既含σ键又含π键
B.(2013·安徽)CO2分子中的化学键为非极性键
C.(2013·四川)NH3分子中N原子的杂化轨道类型是sp2
D.(2013·重庆)沸点:PH3>NH3>H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
四种非金属主族元素M、X、Y、Z在周期表中相对位置如图,下列判断不正确的是
| X | ||
| Y | ||
| Z | M |
A.Z的氢化物中中心原子的杂化方式为sp3
B.Z原子的第一电离能小于M原子的第一电离能
C.四种元素全部位于p区
D.M、Y、Z最高价氧化物对应水化物的酸性从强到弱的顺序为:Y>M>Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com