
µāÓėĒāĘų·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ
¢ŁI2(g)+H2(g) 2HI(g) ¦¤H= - 9.48 kJ”¤mol-1
2HI(g) ¦¤H= - 9.48 kJ”¤mol-1
¢ŚI2(s)+H2(g) 2HI(g) ¦¤H= + 26.48 kJ”¤mol-1£¬ÓÉ“ĖÅŠ¶ĻĻĀĮŠĖµ·Ø»ņ·“Ó¦ÕżČ·µÄŹĒ
2HI(g) ¦¤H= + 26.48 kJ”¤mol-1£¬ÓÉ“ĖÅŠ¶ĻĻĀĮŠĖµ·Ø»ņ·“Ó¦ÕżČ·µÄŹĒ
A£®·“Ó¦¢ŁµÄ²śĪļ±Č·“Ó¦¢ŚµÄ²śĪļĪȶØ
B£®I2(s) I2(g) ¦¤H= + 17.00 kJ”¤mol-1
I2(g) ¦¤H= + 17.00 kJ”¤mol-1
C£®·“Ó¦¢ŚµÄ·“Ó¦Īļ×ÜÄÜĮæ±Č·“Ó¦¢ŁµÄ·“Ó¦Īļ×ÜÄÜĮæµĶ
D£®1 mol I2(g)ÖŠĶØČė1 mol H2(g)£¬·“Ó¦ŗó·ÅČČ9.48 kJ
 ½ņĒŽĢÓż¼ĘĖ抔דŌŖĻµĮŠ“š°ø
½ņĒŽĢÓż¼ĘĖ抔דŌŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻąĶ¬Ģå»żµÄNaClČÜŅŗ£ØÅضČĪŖC1£©ŗĶNa2SO4ČÜŅŗ£ØÅضČĪŖC2£©£¬ČōĘäÖŠµÄNa+ ĪļÖŹµÄĮæÅضČĻąĶ¬£¬ŌņĖüĆĒµÄĪļÖŹµÄĮæÅضČC1ŗĶC2µÄ¹ŲĻµŹĒ £Ø £©
A£®C1 £¾C2 B£®C1 £½C2 C£®C1 £¼C2 D£®2 C1 £½C2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠŅ»¶ØĮæµÄCuŗĶFe2O3×é³ÉµÄ»ģŗĻĪļ£¬Ę½¾ł·Ö³ÉĮ½µČ·Ö£¬ĻņĘäÖŠŅ»·Ż¼ÓČė2 mol”¤L-1µÄŃĪĖįČÜŅŗ150 mL£¬Ē”ŗĆĶźČ«Čܽā£¬ĖłµĆČÜŅŗ¼ÓČėKSCNĪŽŃŖŗģÉ«³öĻÖ”£ČōÓĆ¹żĮæµÄCOŌŚøßĪĀĻĀ»¹ŌŌ»ģŗĻĪļ£¬¹ĢĢåÖŹĮæ¼õÉŁĪŖ£Ø £©
A. 1.6 g B. 2.4 g C. 3.2 g D. 4.8 g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
·“Ó¦3A(g)+B(g)  2C(g)+2D(g)£¬ŌŚ²»Ķ¬ĒéæöĻĀ²āµĆ·“Ó¦ĖŁĀŹČēĻĀ£¬ĘäÖŠ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ
2C(g)+2D(g)£¬ŌŚ²»Ķ¬ĒéæöĻĀ²āµĆ·“Ó¦ĖŁĀŹČēĻĀ£¬ĘäÖŠ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ
A£®v (A)=0.15 mol”¤L-1”¤s-1 B£®v (B)=0.3 mol”¤L-1”¤s-1
C£®v (C)=0.5 mol”¤L-1”¤s-1 D£®v (D)=0.4 mol”¤L-1”¤s-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
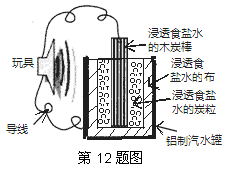 ÓŅĶ¼ŹĒŅ»øöÓĆ·Ļ¾É²ÄĮĻÖĘ×÷µÄæÉÓĆÓŚĒż¶ÆĶę¾ßµÄµē³ŲŹ¾ŅāĶ¼£¬øƵē³Ų¹¤×÷Ź±£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
ÓŅĶ¼ŹĒŅ»øöÓĆ·Ļ¾É²ÄĮĻÖĘ×÷µÄæÉÓĆÓŚĒż¶ÆĶę¾ßµÄµē³ŲŹ¾ŅāĶ¼£¬øƵē³Ų¹¤×÷Ź±£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®Ä¾Ģæ°ōÓ¦ÓėĶę¾ßµē»śµÄøŗ¼«ĻąĮ¬
B£®ĢæĮ£ŗĶĢæ°ōÉĻ·¢ÉśµÄµē¼«·“Ó¦ŹĒ£ŗO2+4e-=2O2-
C£®ĀĮ¹Ž½«Öš½„±»øÆŹ“
D£®ŅņĪŖŅ»æŖŹ¼·“Ó¦¾Ķ»įÉś³É“óĮæĀČĘų£¬øƵē³ŲÓŠŅ»¶Ø
µÄĪ£ĻÕŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©ŅŃÖŖij·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ£ŗK=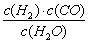 £¬ŌņĖüĖł¶ŌÓ¦·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”ų ”£
£¬ŌņĖüĖł¶ŌÓ¦·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”ų ”£
£Ø2£© ŗĻ³É¼×“¼µÄÖ÷ŅŖ·“Ó¦ŹĒ£ŗ2H2(g)+CO(g) CH3OH(g) ”÷H=-90.8 kJ”¤mol-1£¬t”ęĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżĪŖ160”£“ĖĪĀ¶ČĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠæŖŹ¼Ö»¼ÓČėCO”¢H2£¬·“Ó¦l0minŗó²āµĆø÷×é·ÖµÄÅضČČēĻĀ£ŗ
CH3OH(g) ”÷H=-90.8 kJ”¤mol-1£¬t”ęĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżĪŖ160”£“ĖĪĀ¶ČĻĀ£¬ŌŚĆܱÕČŻĘ÷ÖŠæŖŹ¼Ö»¼ÓČėCO”¢H2£¬·“Ó¦l0minŗó²āµĆø÷×é·ÖµÄÅضČČēĻĀ£ŗ
| ĪļÖŹ | H2 | CO | CH3OH |
| ÅØ¶Č£Ømol/L£© | 0.2 | 0.1 | 0.4 |
£ØA£©øĆŹ±¼ä¶ĪÄŚ·“Ó¦ĖŁĀŹv(H2)= ”ų
£ØB£©±Č½Ļ“ĖŹ±Õż”¢Äę·“Ó¦ĖŁĀŹµÄ“󊔣ŗvÕż ”ų vÄę£ØĢī”°>”±”¢”°<”±»ņ”°=”±£©
£ØC£©·“Ó¦“ļµ½Ę½ŗāŗ󣬱£³ÖĘäĖüĢõ¼ž²»±ä£¬ČōÖ»°ŃČŻĘ÷µÄĢå»żĖõŠ”Ņ»°ė£¬Ę½ŗāĻņ ”ų
(Ģī”°ÄęĻņ”±”¢”°ÕżĻņ”±»ņ”°²»”±)ŅĘ¶Æ£¬Ę½ŗā³£ŹżK ”ų (Ģī”°Ōö“ó”±”¢”°¼õŠ””± »ņ”°²»±ä”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®HNO3µÄĦ¶ūÖŹĮæĪŖ63
B£®Ä¦¶ūŹĒĪļÖŹµÄĮæµÄµ„Ī»
C£®1 molČĪŗĪĪļÖŹ¶¼Ō¼ŗ¬ÓŠ6.02”Į1023øöŌ×Ó
D£®64 g SO2ÖŠŗ¬ÓŠ1mol O2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
æĘѧ¼ŅøÕøÕ·¢ĻÖµÄijÖÖŌŖĖŲµÄŅ»øöŌ×Ó£¬ĘäÖŹĮæŹĒ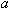 g£¬Ņ»øö12CµÄŌ×ÓÖŹĮæŹĒb g£¬
g£¬Ņ»øö12CµÄŌ×ÓÖŹĮæŹĒb g£¬
ÓĆNAŹĒ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ(””””)
A£®øĆŌ×ÓµÄĦ¶ūÖŹĮæŹĒ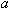 NA g”¤mol-1 B£®WgøĆŌ×ÓÖŠŗ¬ÓŠ
NA g”¤mol-1 B£®WgøĆŌ×ÓÖŠŗ¬ÓŠ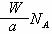 øöŌ×Ó
øöŌ×Ó
C£®WgøĆŌ×ÓµÄĪļÖŹµÄĮæŹĒ 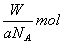 D£®ÓÉŅŃÖŖŠÅĻ¢æÉµĆ£ŗ
D£®ÓÉŅŃÖŖŠÅĻ¢æÉµĆ£ŗ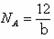 mol-1
mol-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«×ÜĪļÖŹµÄĮæĪŖn molµÄÄĘŗĶĀĮµÄ»ģŗĻĪļ(ĘäÖŠÄʵÄĪļÖŹµÄĮæ·ÖŹżĪŖx)£¬Ķ¶ČėŅ»¶ØĮæµÄĖ®ÖŠ³ä·Ö·“Ó¦£¬½šŹōƻӊŹ£Óą£¬¹²ŹÕ¼Æµ½±ź×¼×“æöĻĀµÄĘųĢåV L ”£ĻĀĮŠ¹ŲĻµŹ½ÖŠÕżČ·µÄŹĒ (””””)
”£ĻĀĮŠ¹ŲĻµŹ½ÖŠÕżČ·µÄŹĒ (””””)
A£®x£½V/(11.2n) B£®0<x”Ü0.5
C£®V£½33.6n(1£x) D£®11.2n<V”Ü22.4n
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com