
【题目】纳米级Cu2O由于具有优良的催化性能而受到科学家的不断关注,下列为制取Cu2O的三种方法:
方法Ⅰ | 用碳粉在高温条件下还原CuO |
方法Ⅱ | 电解法,原理为2Cu+H2O |
方法Ⅲ | 用肼(N2H4)还原新制的Cu(OH)2 |
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是_________________________ 。
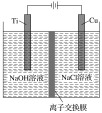
(2)方法Ⅱ利用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为______________________________ ;电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解,通过离子交换膜的阴离子的物质的量为________mol。(离子交换膜只允许OH-通过)
(3)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制的Cu(OH)2来制备纳米级Cu2O,同时放出N2。生成1molN2时,生成Cu2O的物质的量为________________。
(4)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。写出肼-空气燃料电池放电时负极的电极反应式:___________________________。
【答案】反应不易控制,Cu2O可能被C继续还原为Cu2Cu-2e-+2OH-===Cu2O+H2O0.012molN2H4+4OH--4e-=4H2O+N2↑
【解析】
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是C还原CuO生成的Cu2O可能被C继续还原为Cu,反应不易受控制。(2)阳极Cu失去电子发生氧化反应,2Cu-2e-+2OH-=Cu2O+H2O。电池阴极的反应式为2H2O+2e-=H2↑+2OH-,阴极生成的气体为H2,标准状况下生成气体的物质的量为0.005mol,所以通过离子交换膜的阴离子的物质的量为0.01mol。(3)方法Ⅲ的化学反应方程式为N2H4+4Cu(OH)2=2 Cu2O+6H2O+N2↑,由化学方程式可知,生成1molN2时,同时生成Cu2O的物质的量为2mol。(4)燃料负极失去电子发生氧化反应,电极方程式为N2H4+4OH--4e-=4H2O+N2↑。


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列仪器:①漏斗、②冷凝管、③蒸馏烧瓶、④玻璃棒、⑤分液漏斗、⑥锥形瓶,其中蒸馏操作不需要的仪器是( )
A.①③④B.①②⑥C.①④⑤D.②③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:

(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的仪器是________(填序号);

(2)步骤Ⅰ中加入过量铁粉的目的是________;步骤Ⅱ中________(填“能”或“不能”)用盐酸代替硫酸。
(3)步骤Ⅲ的实验装置如图所示,加热装置应与装置________(填“甲”“乙”或“丙”)连接,理由是_____________

(4)利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉,过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。从安全角度考虑,方案________(填“甲”“乙”或“丙”,下同)不好;从产品纯度考虑,方案________不好。
(5)写出步骤Ⅰ中涉及反应的离子方程式:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是
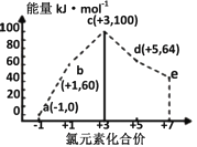
A. a、b、c、d、e中,c最稳定
B. b→a+c反应的活化能为反应物能量减生成物能量
C. b→a+d反应的热化学方程式为:3ClO-(aq)=ClO3-(aq)+2Cl-(aq)ΔH=+116 kJ·mol-1
D. 一定温度下,Cl2与NaOH溶液反应生成的产物有a、b、d,溶液中a、b、d的浓度之比可能为11∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧排放的烟气含有 SO2和 NOx,形成酸雨、污染大气。
(1)采用 NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 SO2和 NO 的烟气,写出 NaClO2溶液脱硝过程中主要反应的离子方程式______________.
(2)NO2与SO2能发生反应:NO2+SO2 ![]() SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:
SO3+NO,在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(N02) : n0 (SO2)] 进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。 部分实验结果如图所示:
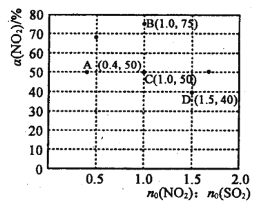
①当容器内________(填标号)不再随时间的变化而改变时,可以判断反应达到了化学平衡状态。
a.气体的压强
b.气体的平均摩尔质量
c.气体的密度
d.N02的体积分数
e.气体的颜色
②如果要将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是__________。
③图中C、D两点对应的实验温度分别为Tc和Td,试判断: Tc_____Td(填“>”、“=”或“<”)。
(3)已知:2NO(g)+O2(g) ![]() 2NO2(g) △H=-113.0 kJ mol-1
2NO2(g) △H=-113.0 kJ mol-1
2SO2(g) + O2(g) ![]() 2SO3(g) △H=-196. 6 kJ mol-1
2SO3(g) △H=-196. 6 kJ mol-1
则 NO2(g)+SO2(g) ![]() SO3(g)+NO(g) △H= ________.
SO3(g)+NO(g) △H= ________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是探究铁发生腐蚀的装置图,下列说法正确的是

A. 若B处液面上升,A溶液可能是酸性溶液
B. 若A为NaCl溶液,B、C液面始终保持不变
C. 可能产生Fe2O3·nH2O
D. 腐蚀的总反应式一定是:2Fe + O2 + 2H2O === 2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:①O2和O3;②![]()
![]()
![]() ;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和
;③H2O、D2O、T2O;④C16H34和(CH3)2CHCH2CH3;⑤CH3(CH2)3CH3和![]() ;⑥2-甲基丁烷、异戊烷。
;⑥2-甲基丁烷、异戊烷。
其中互为同位素的是_______;互为同素异形体的是_______;互为同系物的是_______;互为同分异构体的是_______;属于同种物质的是_______。(用序号填空,下同)
(2)为了研究化学反应A+B===C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题:

①该反应为______反应(填“放热”或“吸热”)。
②A和B的总能量比C和D的总能量___(填“高”或“低”)。
③物质中的化学能通过______转化成______释放出来。
④反应物化学键断裂吸收的能量________(填“高”或“低”)于生成物化学键形成放出的能量。
⑤写出一个符合题中条件的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是
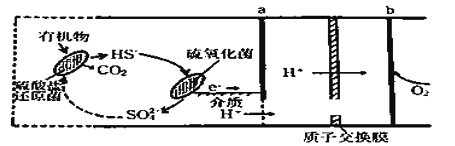
A. HS-在硫氧化菌作用下转化为SO42-的反应为:HS-+4H2O-8e-== SO42-+9H+
B. 电子从b流出,经外电路流向a
C. 如果将反应物直接燃烧,能量的利用率不会变化
D. 若该电池电路中有0.4mol电子发生转移,则有0.45molH+通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应叙述相符的是
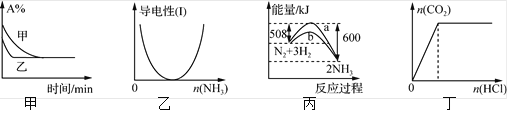
A. 图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
B. 图乙表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C. 图丙表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
D. 图丁表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸物质的量的关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com