
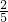 .2mol水参加氧化还原反应,根据氧化还原反应中电子转移守恒计算被水还原的BrF3的物质的量.2mol水参加氧化还原反应,根据氧元素守恒可知,生成氧气1mol,被还原的BrF3生成Br2,根据方程式计算生成溴1mol,利用溴元素守恒被还原的BrF3物质的量.
.2mol水参加氧化还原反应,根据氧化还原反应中电子转移守恒计算被水还原的BrF3的物质的量.2mol水参加氧化还原反应,根据氧元素守恒可知,生成氧气1mol,被还原的BrF3生成Br2,根据方程式计算生成溴1mol,利用溴元素守恒被还原的BrF3物质的量.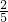 ,所以2mol水参加氧化还原反应,令被水还原的BrF3的物质的量为xmol,根据电子转移守恒,则:
,所以2mol水参加氧化还原反应,令被水还原的BrF3的物质的量为xmol,根据电子转移守恒,则: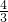 ,
,

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
在反应:3BrF3+5H2O= HBrO3+Br2+9HF十O2中(F为-1价)
(1)此反应中被氧化的元素是 、被还原的元素是 。
(2)当有5mol水参加反应时,被氧化的水的物质的量为 ,被还原的BrF3的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省海安县南莫中学高一上学期期中考试化学试卷 题型:填空题
在反应:3BrF3+5H2O= HBrO3+Br2+9HF十O2中(F为-1价)[来源:学+科+网Z+X+X+K]
(1)此反应中被氧化的元素是 、被还原的元素是 。
(2)当有5mol水参加反应时,被氧化的水的物质的量为 ,被还原的BrF3的物质的量为 。
查看答案和解析>>
科目:高中化学 来源:2010年江苏省高一上学期期中考试化学试卷 题型:填空题
在反应:3BrF3+5H2O= HBrO3+Br2+9HF十O2中(F为-1价)[来源:学+科+网Z+X+X+K]
(1)此反应中被氧化的元素是 、被还原的元素是 。
(2)当有5mol水参加反应时,被氧化的水的物质的量为 ,被还原的BrF3的物质的量为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com