
| A”¢Ģ½¾æ²»Ķ¬“߻ƼĮ¶ŌĶ¬Ņ»·“Ó¦ĖŁĀŹµÄÓ°Ļģ | B”¢Ģ½¾æĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāµÄÓ°Ļģ |
 ŹŌ¼Į£ŗµķ·ŪČÜŅŗ”¢µāĖ®”¢ ĶŁŅŗ”¢2mol/L H2SO4ČÜŅŗ ĻÖĻó£ŗĶ¼ÖŠ×óŹŌ¹ÜČÜŅŗŃÕÉ«Ņ»¶ĪŹ±¼äŗóÖš½„±äĄ¶É«£¬ÓŅŹŌ¹ÜČÜŅŗŃÕÉ«ŃøĖŁ±äĄ¶É« | 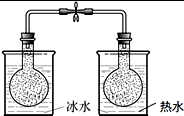 2NO2£Øg£©?N2O4”÷H£¼0 ŹŌ¼Į£ŗÉÕĘæÖŠø÷³äČėµČÖŹĮæµÄNO2 ĻÖĻó£ŗŅ»¶ĪŹ±¼äŗó£¬ÓŅ±ßÉÕĘæÄŚĘųĢåŃÕÉ«±äĒ³£¬×ó±ßÉÕĘæÄŚĘųĢåŃÕÉ«±äÉī |
| C”¢Ģ½¾æ“×Ėį”¢Ģ¼Ėį”¢ÅšĖįµÄĖįŠŌĒæČõ | D”¢ŃéÖ¤Ķā¼ÓµēĮ÷µÄŅõ¼«±£»¤·Ø |
 ŹŌ¼Į£ŗ0.1mol/L“×ĖįČÜŅŗ”¢±„ŗĶÅšĖį ČÜŅŗ0.1mol/L Na2CO3ČÜŅŗ ĻÖĻó£ŗĶ¼ÖŠ×óŹŌ¹ÜÄŚŅŗĆę²śÉśĘųÅŻ£¬ÓŅŹŌ¹ÜĪŽĆ÷ĻŌĻÖĻó | 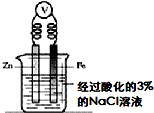 ŹŌ¼Į£ŗĖį»ÆµÄ3%µÄNaClČÜŅŗ”¢ ĢśĒč»Æ¼ŲČÜŅŗ ĻÖĻó£ŗŅ»¶ĪŹ±¼äŗó£¬ĻņÉÕ±ÖŠµĪ¼Ó2µĪĢśĒč»Æ¼ŲČÜŅŗ£¬²»²śÉśĄ¶É«³Įµķ |
| A£® | A | B£® | B | C£® | C | D£® | D |
·ÖĪö A£®µāÓöµķ·ŪŹŌŅŗ±äĄ¶É«£¬µķ·ŪĖ®½āÉś³ÉĘĻĢŃĢĒŹ±£¬ČÜŅŗĶŹÉ«£»
B.2NO2£Øg£©?N2O4µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬½µµĶĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£»
C£®ĒæĖįÄÜŗĶČõĖįŃĪ·“Ӧɜ³ÉČõĖį£»
D£®ŅŖŃéÖ¤Ķā¼ÓµēĮ÷µÄŅõ¼«±£»¤·Ø£¬Ó¦øĆ½«µē¼«Į¬½ÓĶā¼ÓµēŌ“£®
½ā“š ½ā£ŗA£®µāÓöµķ·ŪŹŌŅŗ±äĄ¶É«£¬µķ·ŪĖ®½āÉś³ÉĘĻĢŃĢĒŹ±£¬ĘĻĢŃĢĒŗĶµā²»·“Ó¦£¬ĖłŅŌČÜŅŗĶŹÉ«£¬ĻÖĻó“ķĪ󣬹ŹA“ķĪó£»
B.2NO2£Øg£©?N2O4µÄÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāÄęĻņŅĘ¶Æ£¬½µµĶĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£¬ĖłŅŌŅ»¶ĪŹ±¼äŗó£¬ÓŅ±ßÉÕĘæÄŚĘųĢåŃÕÉ«±äÉī£¬×ó±ßÉÕĘæÄŚĘųĢåŃÕÉ«±äĒ³£¬ĻÖĻó“ķĪ󣬹ŹB“ķĪó£»
C£®ĒæĖįÄÜŗĶČõĖįŃĪ·“Ӧɜ³ÉČõĖį£¬“×ĖįŗĶĢ¼ĖįÄĘ·“Ӧɜ³É¶žŃõ»ÆĢ¼£¬Ģ¼ĖįÄĘŗĶÅšĖį²»·“Ó¦£¬ĖłŅŌĖįŠŌ“×Ėį£¾Ģ¼Ėį£¾ÅšĖį£¬¹ŹCÕżČ·£»
D£®ŅŖŃéÖ¤Ķā¼ÓµēĮ÷µÄŅõ¼«±£»¤·Ø£¬Ó¦øĆ½«µē¼«Į¬½ÓĶā¼ÓµēŌ“£¬øĆŹµŃéŃéÖ¤µÄŹĒĪžÉüŃō¼«µÄŅõ¼«±£»¤·Ø£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧŹµŃé·½°øĘĄ¼Ū£¬ĪŖøßĘµæ¼µć£¬Éę¼°½šŹōµÄøÆŹ“Óė·Ą»¤”¢ĖįŠŌĒæČõÅŠ¶Ļ”¢ĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāŅʶÆÓ°Ļģ”¢ĪļÖŹ¼ģŃéµČÖŖŹ¶µć£¬Ć÷Č·ĪļÖŹŠŌÖŹ¼°ŹµŃéŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬×¢Ņā“ÓĘĄ¼ŪŠŌ·ÖĪö½ā“š£¬ŅדķŃ”ĻīŹĒAD£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| MnO2 | “„ĆžŹŌ¹ÜĒéæö | ¹Ū²ģ½į¹ū | ·“Ó¦Ķź³ÉĖłŠčµÄŹ±¼ä |
| ·Ūĩד | ŗÜĢĢ | ¾ēĮŅ·“Ó¦£¬“ų»šŠĒµÄľĢõø“Č¼ | 3.5 min |
| æéד | Ī¢ČČ | ·“Ó¦½ĻĀż£¬»šŠĒŗģĮĮµ«Ä¾ĢõĪ“ø“Č¼ | 30min |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 µÄĖµ·Ø£¬²»ÕżČ·µÄŹĒ£Ø””””£©
µÄĖµ·Ø£¬²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ¼Čæɓ߻ƼÓĒā£¬ÓÖÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ« | |
| B£® | æÉÓėÅØäåĖ®·¢Č”“śÉś·“Ó¦£¬µ«²»ÄÜ·¢ÉśĻūČ„·“Ó¦ | |
| C£® | 1moløĆ»ÆŗĻĪļ×ī¶ąæÉÓė10molNaOH·“Ó¦ | |
| D£® | æÉÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬²»ÓėNaHCO3·“Ó¦·Å³öCO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
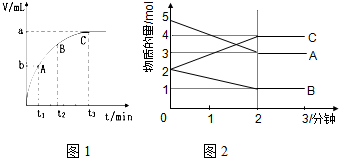
 ÄæĒ°£¬Ęū³µ³§ÉĢ³£ĄūÓĆ“ß»Æ¼¼Źõ½«Ī²ĘųÖŠµÄNOŗĶCO×Ŗ»Æ³ÉCO2ŗĶN2£¬»Æѧ·½³ĢŹ½ČēĻĀ£ŗ2NO+2CO$\stackrel{“߻ƼĮ}{?}$2CO2+N2£®ĪŖŃŠ¾æČēŗĪĢįøßøĆ×Ŗ»Æ¹ż³Ģ·“Ó¦ĖŁĀŹ£¬Ä³æĪĢā×é½ųŠŠĮĖŅŌĻĀŹµŃéĢ½¾æ£®
ÄæĒ°£¬Ęū³µ³§ÉĢ³£ĄūÓĆ“ß»Æ¼¼Źõ½«Ī²ĘųÖŠµÄNOŗĶCO×Ŗ»Æ³ÉCO2ŗĶN2£¬»Æѧ·½³ĢŹ½ČēĻĀ£ŗ2NO+2CO$\stackrel{“߻ƼĮ}{?}$2CO2+N2£®ĪŖŃŠ¾æČēŗĪĢįøßøĆ×Ŗ»Æ¹ż³Ģ·“Ó¦ĖŁĀŹ£¬Ä³æĪĢā×é½ųŠŠĮĖŅŌĻĀŹµŃéĢ½¾æ£®| ŹµŃ鱹ŗÅ | ŹµŃéÄæµÄ | T/”ę | NO³õŹ¼ÅØ¶Č mol/L | CO³õŹ¼ÅØ¶Č mol/L | Ķ¬Ö֓߻ƼĮµÄ±Č±ķĆ껿m2/g |
| ¢ń | ĪŖŅŌĻĀŹµŃé×÷²ĪÕÕ | 280 | 6.50”Į10-3 | 4.00”Į10-3 | 80 |
| ¢ņ | Ģ½¾æ“߻ƼĮ±Č±ķĆ껿¶ŌĪ²Ęų×Ŗ»ÆĖŁĀŹµÄÓ°Ļģ | 280 | 6.50”Į10-3 | 4.00”Į10-3 | 120 |
| ¢ó | Ģ½¾æĪĀ¶Č¶ŌĪ²Ęų×Ŗ»ÆĖŁĀŹµÄÓ°Ļģ | 360 | 6.50”Į10-3 | 4.00”Į10-3 | 80 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ӣ
”¢ £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | X”¢Y”¢ZŌŖĖŲ·Ö±šĪŖN”¢P”¢O | |
| B£® | °×øńÖŠ¶¼ŹĒÖ÷×åŌŖĖŲ£¬»ŅøńÖŠ¶¼ŹĒø±×åŌŖĖŲ | |
| C£® | Ō×Ó°ė¾¶£ŗZ£¾X£¾Y | |
| D£® | X”¢Y”¢ZµÄĘųĢ¬Ēā»ÆĪļÖŠ×īĪČ¶ØµÄŹĒ£ŗXµÄĒā»ÆĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com