
| A. | 四氯化碳分子的比例模型: | B. | 如图所示一定代表丙烯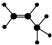 | ||
| C. | 12C32S2比12C34S2更易挥发 | D. | O${\;}_{2}^{2-}$电子式为: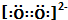 |
分析 A.Cl原子半径大于C原子;
B.硅也能成四个共价键;
C.利用相对分子质量来比较分子晶体的沸点,沸点低的容易蒸发;
D.根据过氧根中,氧原子之间形成的是非极性共价单键,并且均达到了8电子稳定结构知识来回答.
解答 解:A.Cl原子半径大于C原子,四氯化碳分子比例模型不正确,比例模型应符合原子的大小,其正确的比例模型为: ,故A错误;
,故A错误;
B.硅也能成四个共价键,故此球棍模型不一定是丙烯,故B错误;
C.因12C32S2的相对分子质量32×2+12=76,12C34S2的相对分子质量为34×2+12=80,则12C32S2的沸点低,12C32S2在相同条件下比12C34S2更易挥发,故C正确;
D.过氧根中,氧原子之间形成的是非极性共价单键,并且有1对共用电子,故D错误,
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及离子结构示意图、电子式、比例模型、结构式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生规范答题的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质生成的反应一定是氧化还原反应 | |
| B. | 分解反应和复分解反应都不是氧化还原反应 | |
| C. | 氧化还原反应中一定有电子发生转移 | |
| D. | 置换反应也有可能是非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
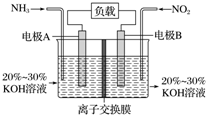 利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )
利用反应6NO2+8NH3═7N2+12H2O构成电池的方法,既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,下列说法不正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 为使电池持续放电,离子交换膜需选用阴离子交换膜 | |
| C. | 电极A极反应式为2NH3-6e-+6OH-═N2+6H2O | |
| D. | 当有4.48 L NH3 (标准状况)反应时,转移电子为0.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
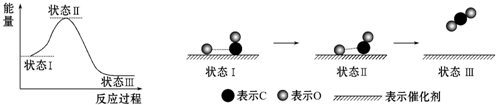
| A. | CO和O生成CO2是吸热反应 | |
| B. | 在该过程中,CO断键形成C和O | |
| C. | 状态Ⅰ→状态Ⅲ表示CO和O反应生成CO2的过程 | |
| D. | 状态Ⅰ→状态Ⅲ表示CO与O2反应生成CO2的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量 M=$\frac{22.4mw}{[(1-w)V]}$ | B. | 物质的量浓度 c=$\frac{1000dV}{(MV+22.4m)}$ | ||
| C. | 溶质的质量分数 w=$\frac{MV}{22.4m}$ | D. | 溶液密度 d=$\frac{cM}{1000w}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com