
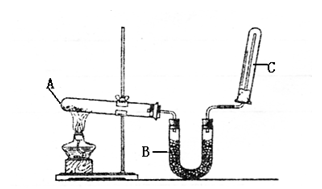
| A.a1=2a2 | B.2a2>a1 | C.a1>2a2 | D.无法确定 |
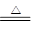 CaCl2+2H2O+2NH3↑
CaCl2+2H2O+2NH3↑

 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
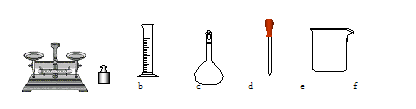
| A.称取8.0g胆矾,在480mL /c中定容 |
| B.称取12.5g胆矾,在500mL /e中定容 |
| C.称取8.0g硫酸铜,在500mL /c中定容 |
| D.称取12.50g胆矾,在500mL /c中定容 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
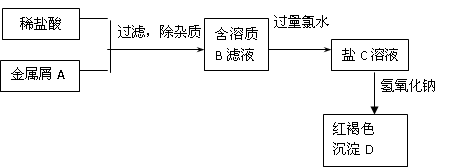
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
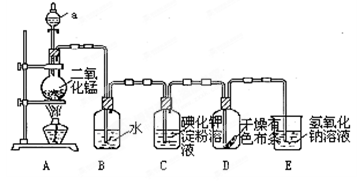
 MnCl2+2H2O+ Cl2↑
MnCl2+2H2O+ Cl2↑查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
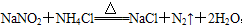 ,关于该反应的说法正确的是( )
,关于该反应的说法正确的是( )| A.生成1 molN2时转移的电子为6 mol | B.NaNO2是氧化剂 |
| C.NH4Cl中的N元素被还原 | D.N2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 =3I2+3H2O+3K2SO4
=3I2+3H2O+3K2SO4 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com