
| A. | 液化、汽化、风化、熔化等都属于物理变化 | |
| B. | 液化石油气、汽油、花生油主要成分都是碳氢化合物 | |
| C. | 水分子之间可以形成氢键,所以水比硫化氢稳定 | |
| D. | 提出原子在一定轨道上运动的原子结构模型是波尔 |
分析 A、风化是失去全部结晶水或部分结晶水,生成了新的物质,属于化学变化;
B、花生油是油脂是烃的含氧衍生物;
C、氢键是决定物质的物理性质,而稳定性是化学性质;
D、波尔提出原子结构轨道模型.
解答 解:A、碳酸钠晶体的风化是失去全部结晶水或部分结晶水,生成了新的物质,属于化学变化,故A错误;
B、花生油是油脂,故B错误;
C、氢键是决定物质的物理性质,而稳定性是化学性质,由氢氧共价键的强弱决定,故C错误;
D、波尔提出原子结构轨道模型,故D正确;
故选:D.
点评 清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水和酸性高锰酸钾溶液褪色 |
| B | Fe3+有强氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
| C | 浓硫酸有吸水性 | 浓硫酸可使蔗糖和纸张碳化变黑 |
| D | SiO2有导电性 | SiO2可用于制备光导纤维 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸乙酯、油脂都属于酯类,但不是同系物 | |
| B. | 误服重金属盐,立即服用豆浆或牛奶可解毒 | |
| C. | 蔗糖、纤维素、淀粉水解的最终产物都是葡萄糖 | |
| D. | 煤的干馏可以得到苯等芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .已知反应④为取代反应,写出该反应的化学方程式CH3OH+
.已知反应④为取代反应,写出该反应的化学方程式CH3OH+ $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ +HCl.
+HCl. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.1mol•L-1 HA溶液与0.1 mol•L-1的NaOH溶液中,水电离出来的c(H+)相等 | |
| B. | 混合后溶液中:c(HA)>c(Na+)>c(A-)>c(OH-) | |
| C. | 混合后溶液中:c(A-)+c(HA)=0.2 mol•L-1 | |
| D. | 混合后溶液中:c(Na+)+c(H+)=c(A-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
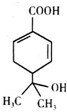
| A. | 分子式为C10H13O3 | |
| B. | 含有两种官能团,可使溴水和酸性高锰酸钾溶液褪色 | |
| C. | 能发生加成、取代、氧化等反应 | |
| D. | 与钠和氢氧化钠溶液都能发生反应,且得到的产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照相器材等领域亦有广泛应用.回答下列问题:
银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照相器材等领域亦有广泛应用.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com