
| A. | 分液漏斗中盛放液体的总体积不得超过其容量的$\frac{2}{3}$ | |
| B. | 某学生用广泛pH试纸测得某溶液的pH为0 | |
| C. | 实验室制取乙酸乙酯用稀硫酸做催化剂效果会更好 | |
| D. | 焰色反应实验,所用铂丝先用盐酸洗涤并在酒精灯火焰上灼烧 |
分析 A.分液漏斗中液体体积不能超出容器容积的$\frac{1}{3}$;
B.广泛pH试纸可在1~14的pH范围内使用;
C.浓硫酸有吸水性;
D.用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用,去除了其它离子的干扰.
解答 解:A.装液时,分液漏斗中液体的总体积不得超过其容器的三分之一,若过多,不能充分萃取,故A错误;
B.广泛pH试纸可在1~14的pH范围内使用,不可能pH为0,故B错误;
C.浓硫酸有吸水性,可使平衡向右移动,故C错误;
D.用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用,去除了其它离子的干扰,且HCL受热以后会挥发,无残留,故D正确.
故选D.
点评 本题考查常见仪器的使用和化学基本操作的方法,题目难度不大,注意在学习中加强基础知识的积累,C为易错点,注意浓硫酸的作用.


科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向沸水中滴加饱和氯化铁溶液,可以制备氢氧化铁胶体,有净水的功能 | |
| B. | 容量瓶、滴定管使用前均需要检漏,并需要润洗以减小实验误差 | |
| C. | 甲烷中混有的少量乙烯可以通过溴水洗涤净化 | |
| D. | 分离乙酸乙酯和乙酸混合液时,先加入一定量的氢氧化钠溶液,生成乙酸钠后进行蒸馏,然后在乙酸钠溶液中加入足量的硫酸再蒸馏可得乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 长期使用(NH4)2SO4化肥会使土壤酸化,而过度使用尿素[CO(NH2)2]会使土壤碱化 | |
| B. | 锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 | |
| C. | 铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝单质 | |
| D. | “酸可以除锈”、“热的纯碱溶液去油污”,都发生了化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 往密闭容器中通入一定量N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,气体颜色变深.如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律.X、Y分别是( )
往密闭容器中通入一定量N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,气体颜色变深.如图表示该反应平衡时有关物理量Y随某条件X(其他条件不变)变化的规律.X、Y分别是( )| A. | 温度T,逆反应速率υ逆 | B. | 温度T,气体的密度ρ | ||
| C. | 压强P,平衡常数K | D. | 压强P,N2O4转化率α |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X:3s23p1 Y:3s23p5 | B. | X:2s22p3 Y:2s22p4 | ||
| C. | X:3s23p1 Y:2s22p5 | D. | X:2s22p3 Y:1s1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
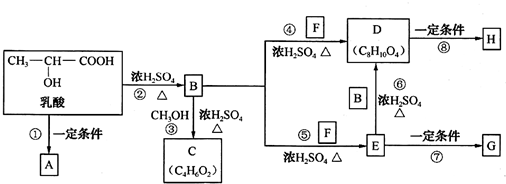
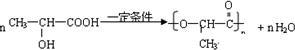 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com