
【题目】将足量X气体通入Y溶液中,实验结果与预测的现象一致的组合是( )
X气体 | Y溶液 | 预测的现象 |
| |
① | CO2 | 饱和Na2CO3溶液 | 白色沉淀析出 | |
② | SO2 | Ba(NO3)2溶液 | 白色沉淀析出 | |
③ | NH3 | AgNO3溶液 | 白色沉淀析出 | |
④ | NH3 | AlCl3溶液 | 白色沉淀析出 |
A.①②③
B.①②④
C.①③④
D.①②③④
【答案】B
【解析】解:①二氧化碳和碳酸钠反应生成碳酸氢钠,碳酸氢钠的溶解性小于碳酸钠的溶解性,所以向饱和的碳酸钠溶液中通入适量的二氧化碳发生Na2CO3+CO2+H2O=2NaHCO3↓,会出现白色沉淀析出,故①正确;②SO2通入水中生成H2SO3 , 溶液呈酸性,NO3﹣在酸性条件下具有强氧化性,可发生3SO2+2H2O+2NO3﹣+3Ba2+=3BaSO4↓+4H++2NO↑,会出现白色沉淀析出,故②正确;③AgNO3溶液与氨水反应生成氢氧化银沉淀,氢氧化银再和氨水发生络合反应生成可溶性络合物,现象为:先产生白色沉淀,然后沉淀逐渐溶解,故③错误;④弱碱不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为AlCl3+3NH3H2O═Al(OH)3↓+3NH4Cl,会出现白色沉淀析出,故④正确; 故选B.


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A. 2-甲基丙烷的一氯代物只有一种 B. 戊烷(C5H12)有两种同分异构体
C. 乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 D. 乙烯、聚氯乙烯和苯分子均含有碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如图所示. 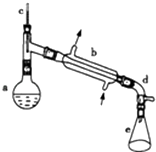
可能用到的有关数据如下:
相对分子质量 | 密度/(gcm﹣3) | 沸点/℃ | 溶解性 | |
环乙醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸.b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.反应粗产物倒入f中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙.最终通过蒸馏得到纯净环己烯.
回答下列问题:
(1)由环己醇制取环己烯的方程式;
(2)装置b的冷凝水方向是(填下进上出或上进下出);
(3)加入碎瓷片的作用是;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验中最容易产生的副产物所含的官能团名称为 .
(5)在分离提纯中,使用到的仪器f名称是 , 分离氯化钙的操作是 .
(6)合成过程中加入浓硫酸的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,必须加入还原剂才可以实现的是( )
A. KC1O3→KC1B. CO→CO2C. Fe2(SO4)3→FeSO4D. Na2O2→NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关酸雨的说法中不正确的是 ( )
A.酸雨形成的主要原因是工业和民用上大量燃烧含硫的化石燃料
B.二氧化碳是形成酸雨的主要物质
C.用天然气代替含硫的煤作燃料,可有效控制酸雨的形成
D.酸雨能直接破坏农作物,使土壤酸性增强,腐蚀建筑物及工业设备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料.用A和常见的有机物可合成一种醚类香料和一种缩醛类香料.具体合成路线如图所示(部分反应条件略去): 
已知:
① ![]()
![]() 2ROH+
2ROH+ ![]()
②D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子,D中氧元素的质量分数约为13.1%.回答下列问题:
(1)C中官能团名称是 , 图中缩醛的分子式是 .
(2)B的结构简式为
(3)⑥的反应类型是 .
(4)⑤的化学方程式为 .
(5)请写出核磁共振氢谱有4组峰,峰面积之比为3:2:2:1,且含有苯环和羰基的苯乙醛的所有同分异构体的结构简式: .
(6)参照  的合成路线,设计一条由2﹣氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2﹣氯丙烷和必要的无机试剂制备  的合成路线(须注明必要的反应条件) .
的合成路线(须注明必要的反应条件) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某些资料认为:NO、NO2不能与Na2O2反应.某小组学生提出质疑,他们从理论上分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设: 假设Ⅰ.过氧化钠氧化二氧化氮
假设Ⅱ.二氧化氮氧化过氧化钠
(1)小组甲同学设计实验如下(图1):①试管A中反应的化学方程式是 ②待试管B中收集满气体,向试管B中加入适量 Na2O2粉末,塞紧塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将余烬木条迅速伸进试管内,看见木条复燃.甲同学认为假设Ⅱ正确;乙同学认为该装置不能达到实验目的,为达到实验目的,在A、B之间增加一个装置,该装置的作用是 .
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;
余烬木条未复燃.得出结论:假设Ⅰ正确.NO2和Na2O2反应的方程式是 .
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化.查阅资料: ①2NO+Na2O2═2NaNO2
②6NaNO2+3H2SO4═3Na2SO4+2HNO3+4NO↑+2H2O;
③酸性条件下,NO或NO2﹣都能与MnO4﹣反应生成NO3﹣和Mn2+
丙同学用如图2所示装置(部分夹持装置略)探究NO与Na2O2的反应.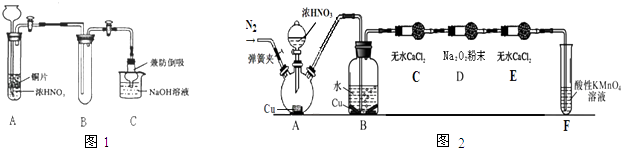
①B中观察到的主要现象是 , F装置的作用是 .
②在反应前,打开弹簧夹,通入一段时间N2 , 目的是 .
③充分反应后,检验D装置中发生反应的实验是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A.聚丙烯的结构简式: ![]()
B.丙烷分子的比例模型: ![]()
C.四氯化碳分子的电子式: ![]()
D.2﹣乙基﹣1,3﹣丁二烯分子的键线式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能说明苯分子中碳碳键不是单、双键交替的事实是
①苯不能使KMnO4溶液褪色;
②苯环中碳碳键的键长均相等;
③邻二氯苯只有一种;
④在一定条件下苯与H2发生加成反应生成环己烷。
A. ①②③④ B. ①②③ C. ②③④ D. ①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com