
| A. | a+b<c | B. | 平衡向正反应方向移动 | ||
| C. | A的转化率降低 | D. | C的体积分数增大 |
分析 反应aA(g)+bB(g)?cC(g)平衡时测得B的浓度为0.6mol/L,保持温度不变,将容器的容积扩大到原来的两倍,若平衡不移动,B的浓度为0.3mol/L,而再达平衡时,测得B的浓度为0.40mol/L,则说明体积增大(压强减小)化学平衡逆向移动,以此来解答.
解答 解:反应aA(g)+bB(g)?cC(g)平衡时测得B的浓度为0.6mol/L,保持温度不变,将容器的容积扩大到原来的两倍,若平衡不移动,B的浓度为0.3mol/L,而再达平衡时,测得B的浓度为0.40mol/L,则说明体积增大(压强减小)化学平衡逆向移动,
A、减小压强平衡向气体体积增大的方向移动,所以a+b>c,故A错误;
B、平衡逆向移动,故B错误;
C、平衡逆向移动,A的转化率降低,故C正确;
D、平衡逆向移动,C的体积分数减小,故D错误;
故选C.
点评 本题考查化学平衡的移动,注意A的浓度变化及体积变化导致的平衡移动是解答本题的关键,熟悉压强对化学平衡的影响即可解答,题目难度不大.


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | NO3-、K+、Cl-、Na+ | D. | HCO3-、K+、NO3-、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol CH4的质量和O2的摩尔质量都是32g | |
| B. | 1 mol任何气体中都含有相同的原子数 | |
| C. | 1 mol NaCl中含有6.02×1023个微粒 | |
| D. | H3PO4的摩尔质量是98.0g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醇的官能团是羟基(-OH) | B. | 烯烃的官能团碳碳双键 | ||
| C. | 甲醛的官能团是醛基(-COH) | D. | 酚的官能团是羟基(-OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含中子数为8NA | |
| B. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| C. | 常温常压下,0.3molCl2通入水中,充分反应后转移电子数目为0.3 NA | |
| D. | 1.0L1.0mo1•L1的NaAlO2水溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(Y)>r(Z)>r(W) | |
| B. | 简单气态氢化物的热稳定性:Y<Z | |
| C. | 氧化物的水化物的酸性:Z<W | |
| D. | X的简单氢化物与W的氢化物相遇可产生白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ | B. | Mg2+ | C. | Fe2+ | D. | Ba2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
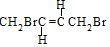 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com