
| A、Na+、HCO3-、Cl- |
| B、Cu2+、Na+、SO42- |
| C、K+、SO42-、OH- |
| D、Fe2+、Al3+、NO3-、H+ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、12.5g |
| B、13.2g |
| C、11.2g |
| D、24.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温高压 |
| 催化剂 |
| A、该反应为可逆反应,故在一定条件下氮气和氢气不可能全部转化为氨气 |
| B、达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C、一定条件下,向某密闭容器中加入1mol N2和3mol H2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等 |
| D、在利用上述反应生产氨气时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、适当升高温度 |
| B、加入NaOH固体 |
| C、通入NH3 |
| D、加入NH4Cl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
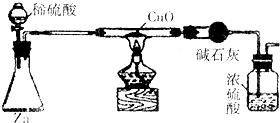 实验室利用下列装置(夹持仪器略)测定水中氢、氧元素的质量比,测得反应前后硬质玻璃管的质量分别为a、b,球形干燥管的质量分别为c、d下列叙述错误的是( )
实验室利用下列装置(夹持仪器略)测定水中氢、氧元素的质量比,测得反应前后硬质玻璃管的质量分别为a、b,球形干燥管的质量分别为c、d下列叙述错误的是( )| A、实验结果表示式为:m(H):m(O)=(d-c-a+b):(a-b) | ||
| B、实验结果m(H):m(O)>1:8,即测定结果偏大 | ||
| C、实验开始时必须先通入H2,完全排除装置中的空气,然后加热 | ||
D、实验结果表示式为:m(H):m(O)=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、市场上假酒销售时有发生,假酒的有毒成分主要是甲醇 |
| B、由石油分馏可获得汽油、煤油、柴油等,可用作燃料和煤油还可保存少量金属钠 |
| C、甲醛水溶液可以用来作食品防腐剂 |
| D、遵守《保护臭氧层维也纳公约》,限制生产和销售氟里昂可减少对大气臭氧层的破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都呈红褐色 |
| B、向Fe(OH)3胶体中滴加几滴浓盐酸,可能看到有沉淀产生 |
| C、利用滤纸过滤的方法可以分离两者 |
| D、微粒大小都在1~100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1Llmol/L醋酸溶液中离子总数为2NA |
| B、标准状况下,2.24L的己烷中含有C-H键的数目为0.6NA |
| C、常温常压下,1mol苯含C=C为3NA |
| D、乙烯和丙烯的混合物1.4g中含有0.1NA个碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Be2+中的电子数和质子数之比一定为1:2 |
| B、D216O中,质量数之和是质子数之和的两倍 |
| C、在氮原子中,质子数为7而中子数不一定为7 |
D、Cl-的结构示意图为: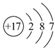 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com