
| ѡ�� | �Լ� | ���������� |
| A | AgNO3��Һ | �μӰ�ˮ�����������������μӰ�ˮ�������ܽ� |
| B | ���� | �μ�NaOH��Һ���������壻�����μӣ�������ɫ���� |
| C | CuSO4��Һ | �ӹ���NaOH��Һ��������ɫ�������ټ���ȩ�����ȣ�������ɫ���� |
| D | ��ˮ | �μ�NaOH��Һ����Һ��ɫ��ȥ���ټ�HCl����Һ��ɫ�ָ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��������AgOH��������������Һ��
B��Al��NaOH��Һ��Ӧ����ƫ�����ƺ�������
C��������������ͭ�������ټ���ȩ������������Ӧ����������ͭ��
D����ˮ��NaOH��Ӧ�����κ�ˮ���ټ����ᣬ����������Cl-��ClO-����������ԭ��Ӧ����������
��� �⣺A��������AgOH��������������Һ������������Һ�еμӰ�ˮ�����������������μӰ�ˮ�������ܽ⣬��A��ȷ��
B��Al��NaOH��Һ��Ӧ����ƫ�����ƺ����������NaOH����ʱ�������ɰ�ɫ��������B����
C��������������ͭ�������ټ���ȩ������������Ӧ����������ͭ��������ͭ��Һ�мӹ���NaOH��Һ��������ɫ�������ټ���ȩ�����ȣ�������ɫ��������C��ȷ��
D����ˮ��NaOH��Ӧ�����κ�ˮ���ټ����ᣬ����������Cl-��ClO-����������ԭ��Ӧ��������������ˮ�еμ�NaOH��Һ����Һ��ɫ��ȥ���ټ�HCl����Һ��ɫ�ָ�����D��ȷ��
��ѡB��
���� ���⿼�黯ѧʵ�鷽�����ۣ�Ϊ��Ƶ���㣬�������ʵ����ʼ��仯�������������Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ��������Է�������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.8g H218O�к��е�������ΪNA | |
| B�� | 1mol Fe��������Ũ���ᷴӦ������SO2�ķ�����ΪNA | |
| C�� | 7.1g Cl2����ˮ������Һ�к��е�Cl-��ĿΪ0.1NA | |
| D�� | ����ȼ�ϵ�ظ�������2.24L����״��������ʱ����·��ת�Ƶ�����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij�¶���ˮ�����ӻ�����ΪKw���ڸ��¶��£�a mol•L-1һԪ��HA��b mol•L-1һԪ��BOH�������ϣ���Һ�����ԣ�����Һ��c��H+��=$\sqrt{Kw}$ | |
| B�� | ��֪MgCO3��Ksp=6.82��10-6mol2•L-2�����ں��й���MgCO3��Na2CO3��Һ�У���c��Mg2+��=c��CO32-������c��Mg2+��•c��CO32-��=6.82��10-6mol2•L-2 | |
| C�� | Ksp��AB2��С��Ksp��CD����˵��AB2���ܽ��С��CD���ܽ�� | |
| D�� | NH4Cl��NH3•H2O�Ļ����Һ�У��ֱ����NH4+��ˮ��ƽ���NH3•H2O�ĵ���ƽ�⣬���߶ԶԷ���ƽ�ⶼ���˴ٽ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
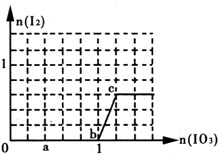
| A�� | a��ʱ����NaHSO3�����ʵ���Ϊ1.2 mol���õ�����������ΪSO42- | |
| B�� | b��c�εķ�Ӧ�����������ӷ���ʽ��ʾ��IO3-+5 I-+6H+�T3I2+3H2O | |
| C�� | �μӹ�����ˮ�ĵ���ƽ��һֱ�����ƶ� | |
| D�� | ��c������û��Һ�з������IJ���Ϊ�������Ȼ�̼��ȡ��Һ��Ȼ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
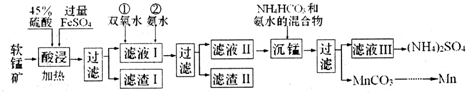
| ���� | Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Al��OH��3 |
| Ksp | 10-13 | 10-17 | 10-39 | 10-33 |
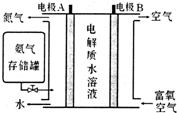
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X�ֱ����������Ԫ�ؾ����γ�����2�ֻ����� | |
| B�� | M��W��X��Y��Z��ԭ�Ӱ뾶�ɴ�С��˳��ΪY��Z��X��W��M | |
| C�� | X��̬�⻯����ȶ��Դ���Z̬�⻯�����X��̬�⻯��ķе�С��Z��̬�⻯�� | |
| D�� | M��X��Y��ɻ������Y��Z��ɻ�������������Ļ�ѧ��������ȫ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHCO3��Һ�ʼ��Ե�ԭ����HCO3-��ˮ��̶ȴ��ڵ���̶� | |
| B�� | ����CaCl2�ٽ���HCO3-�ĵ��� | |
| C�� | ��Ӧ�����ӷ���ʽ��2HCO3-+Ca2+�TCaCO3��+H2CO3 | |
| D�� | ��Ӧ�����Һ�д��ڣ�c��Na+��+2c��Ca2+��=c��HCO3-��+2c��CO32-��+c��Cl-��+c��H2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ó�ϫ�����ǽ���ѧ��ת��Ϊ���� | |
| B�� | ��������ˮ�Ĺ�����һ�������˻�ѧ�仯 | |
| C�� | �Ӻ�ˮ�п��Ի��MgCl2���������MgCl2���Ʊ�Mg | |
| D�� | �����÷�Һ�ķ�������ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
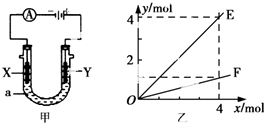
| A�� | ����װ�����ڵ�⾫��ͭ����XΪ��ͭ��YΪ��ͭ��������Һa����������ͭ���Ȼ�ͭ��Һ | |
| B�� | ��ͼ��װ���ö��Ե缫���AgN03��Һ����ͼ�Һ�����x��ʾ����缫�ĵ��ӵ����ʵ�������E�ɱ�ʾ��Ӧ������������ʵ�����F��ʾ���������������ʵ��� | |
| C�� | ��ͼ��װ���ö��Ե缫���һ��Ũ�ȵ�����ͭ��Һ��ͨ��һ��ʱ�����0.5mol��̼��ͭ�պûָ���ͨ��ǰ��Ũ�Ⱥ�pH�����������ת�Ƶĵ���Ϊ2.0 mol | |
| D�� | ��X��YΪ���缫��a��ҺΪ500 mL KCl��KNO3�Ļ��Һ������һ��ʱ����������õ���״����11.2 L���壬��ԭ���Һ��KCl�����ʵ���Ũ������Ϊ2.0 molL-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com