
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
分析 C4H8O2属于羧酸时,可以根据羧基位置异构可以得到丁酸的同分异构体;C4H8O2属于酯类的同分异构体,为饱和一元酯,羧酸和酯都属于同分异构体,根据酸、酯的种类来确定.
解答 解:C4H8O2属于羧酸时,可以是丁酸或2-甲基丙酸,所以C4H8O2属于羧酸时,共有2种同分异构体;
C4H8O2属于酯类的同分异构体,为饱和一元酯,若为甲酸与丙醇形成的酯,甲酸只有1种结构,丙醇有2种,形成的酯有2种,若为乙酸与乙醇形成的酯,乙酸只有1种结构,乙醇只有1种结构,形成的乙酸乙酯有1种,若为丙酸与甲醇形成的酯,丙酸只有1种结构,甲醇只有1种结构,形成的丙酸甲酯只有1种,所以C4H8O2属于酯类的同分异构体共有4种;综合以上分析,总共有6种,故选C.
点评 本题考查同分异构体的种类,根据官能团异构和位置异构和碳链异构来综合分析同分异构体的种数,难度不大,但要注意按照一定的顺序书写同分异构体.


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:解答题
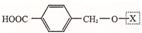 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
 .
.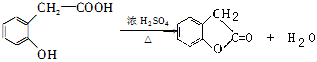 .
.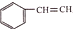 )为主要原料
)为主要原料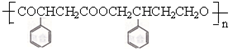 制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$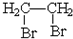 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 科学家在宇宙深处发现了H3+与H3,二者互为同位素 | |
| B. | 焰色反应实验操作过程中,没有铂丝,也可以用光洁无锈的铁丝代替 | |
| C. | N2的结构式为N≡N,电子式为 | |
| D. | Na+的结构示意图 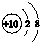 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向溶液X中滴加盐酸无明显现象,再滴加BaCl2溶液有白色沉淀生成,则X中含有SO42- | |
| B. | 向饱和FeCl3溶液中滴加少量氨水,可制取Fe(OH)3胶体 | |
| C. | 检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用KSCN溶液 | |
| D. | 向1mL l% NaOH溶液加入2 mL 2%的CuSO4溶液,振荡后滴加0.5 mL 5%葡萄糖溶液,加热,未出现红色沉淀,证明葡萄糖中不含醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2是白色固体,与冷水作用放出氧气,生成氢氧化钠 | |
| B. | 在Na2O2与CO2的反应中,氧化剂是Na2O2,还原剂是CO2 | |
| C. | Na2O不稳定,能继续被氧化,生成Na2O2 | |
| D. | Na2O2能与水反应,生成NaOH,所以Na2O2是碱性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com