
| A���٢ۢܢ� | B���٢ڢ� |
| C���٢ڢܢ� | D���ڢܢݢ� |
| ||
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| NaOH���������� | �����������ʵ�����/g | �����������ʵ�����/g | |
| A | 0.062��6.2%�� | 19 | 152 |
| B | 0.062��6.2%�� | 152 | 19 |
| C | 0.042��4.2%�� | 1.2 | 9.4 |
| D | 0.042��4.2%�� | 9.4 | 1.2 |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1000 ml |
| B��500 ml |
| C��100 ml |
| D��1500 ml |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ | B����� |
| C���绯ѧ��ʴ | D�������Ļ�ѧ��ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ȼҵ�У����������ڵ��۵����������� |
| B����������������ڹ��������������Ȼ��⣬��ˮ���յõ����� |
| C�����������ڽӴ��ұ��������������������������������ڱ�ˮ�����Ƴ�Ũ���� |
| D���ϳɰ���ҵ�У����ð���Һ���������N2��H2ѭ��ʹ�ã�����������˰��IJ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ�����Һ��c��K+��=1 mol/L |
| B��������������һ��ת�Ƶ���0.8 mol |
| C�����õ���ͭ�����ʵ���Ϊ0.2 mol |
| D��������Һ��c��H+��=2 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
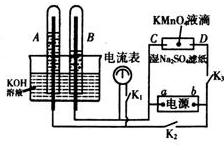 ����ͼ��ʾװ���У��Թ�A��B�еĵ缫Ϊ��Ķ��Ե缫��C��DΪ�������м��ڱ�Na2SO4��Һ��ʪ����ֽ���ϣ���ֽ�����в�����KMnO4Һ�Σ���Դ��a��b��������A��B �г���KOH��Һ������KOH��Һ��ˮ���У��ж�K1���պ�K2��K3��ֱͨ���磮
����ͼ��ʾװ���У��Թ�A��B�еĵ缫Ϊ��Ķ��Ե缫��C��DΪ�������м��ڱ�Na2SO4��Һ��ʪ����ֽ���ϣ���ֽ�����в�����KMnO4Һ�Σ���Դ��a��b��������A��B �г���KOH��Һ������KOH��Һ��ˮ���У��ж�K1���պ�K2��K3��ֱͨ���磮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com