
 ��A��B��C��D��E��ǰ���ڵ�Ԫ�أ�����AԪ�غ�BԪ�ص�ԭ�Ӷ���1��δ�ɶԵ��ӣ�A+��B-��һ�����Ӳ㣬Bԭ�ӵ�һ����������3p�����3p����ѳ�����Cԭ����3�ܼ�������3��δ�ɶԵ��ӣ�D���������������ڲ��������3������̬��E��ǰ��������δ�ɶԵ���������ԭ�ӣ�
��A��B��C��D��E��ǰ���ڵ�Ԫ�أ�����AԪ�غ�BԪ�ص�ԭ�Ӷ���1��δ�ɶԵ��ӣ�A+��B-��һ�����Ӳ㣬Bԭ�ӵ�һ����������3p�����3p����ѳ�����Cԭ����3�ܼ�������3��δ�ɶԵ��ӣ�D���������������ڲ��������3������̬��E��ǰ��������δ�ɶԵ���������ԭ�ӣ����� ��A��B��C��D��E��ǰ���ڵ�Ԫ�أ�����AԪ�غ�BԪ�ص�ԭ�Ӷ���1��δ�ɶԵ��ӣ�Bԭ�ӵ�һ����������3p�����3p����ѳ�������B��ClԪ�أ�
A+��B-��һ�����Ӳ㣬A+ΪNa+���ӣ���A��NaԪ�أ�
Cԭ����3�ܼ�������3��δ�ɶԵ��ӣ�Cԭ�ӵ���Χ�����Ų�Ϊns2np3���ǵڢ�A��Ԫ�أ�AC3����ײ��ʱ�������ֵ��ʣ������������İ�ȫ���ң���C��NԪ�أ�
D���������������ڲ��������3��������������������8������D��OԪ�أ�
��̬��E��ǰ��������δ�ɶԵ���������ԭ�ӣ���E��CrԪ�أ��ٽ����Ŀ�������
��� �⣺��A��B��C��D��E��ǰ���ڵ�Ԫ�أ�����AԪ�غ�BԪ�ص�ԭ�Ӷ���1��δ�ɶԵ��ӣ�Bԭ�ӵ�һ����������3p�����3p����ѳ�������B��ClԪ�أ�
A+��B-��һ�����Ӳ㣬A+ΪNa+���ӣ���A��NaԪ�أ�
Cԭ����3�ܼ�������3��δ�ɶԵ��ӣ�Cԭ�ӵ���Χ�����Ų�Ϊns2np3���ǵڢ�A��Ԫ�أ�AC3����ײ��ʱ�������ֵ��ʣ������������İ�ȫ���ң���C��NԪ�أ�
D���������������ڲ��������3��������������������8������D��OԪ�أ�
��̬��E��ǰ��������δ�ɶԵ���������ԭ�ӣ���E��CrԪ�أ�
��1��E��CrԪ�أ���ԭ��3d��4s����Ϊ��۵��ӣ�3d��4s�ܼ��Ϸֱ���5��1�����ӣ���E�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d54s1���ʴ�Ϊ��3d54s1��
��2��M����Na+��Cl-��ɵĻ����Na+����λ��Ϊ6��NaCl��Na2O�������Ӿ��壬���Ӿ����۷е��뾧���ܳ����ȣ�������������������ɳ����ȡ������Ӱ뾶�ɷ��ȣ�����NaCl�۵�С��Na2O��
�ʴ�Ϊ��6��С�ڣ��Ȼ��������Ӱ뾶����Na2O���������С��Na2O�����Ȼ����۵�С��Na2O��
��3��NaN3����ײ��ʱ�������ֵ���Na�͵����������������İ�ȫ���ң�����ײ��ʱ�����Ļ�ѧ��Ӧ����ʽ��3NaN3$\frac{\underline{\;ײ��\;}}{\;}$Na3N+4N2�����ʴ�Ϊ��3NaN3$\frac{\underline{\;ײ��\;}}{\;}$Na3N+4N2����
��4��ͬһ����Ԫ�أ�Ԫ�صĵ�һ����������ԭ��������������������ƣ�����IIA�塢��VA��Ԫ�ص�һ�����ܴ���������Ԫ�أ�D��OԪ�أ�λ�ڵ�VIA�壬��OԪ����ͬ��������Ԫ�صĵ�һ�������ɴ�С�Ĺ�ϵ��F��N��O���ʴ�Ϊ��F��N��O��
��5������0.0015mol[EBn��H2O��6-n]x+����Һ��R-H��ȫ�������к����ɵ�H+��Ũ��Ϊ0.1200mol•L-1NaOH ��Һ25.00mL��n��NaOH��=0.1200mol/L��0.025L=0.003mol����ΪNaOH�������ӷ�Ӧ��1��1��Ӧ������n��H+��=n��NaOH��=0.003mol�����ݣ�[EBn��H2O��6-n]x++xR-H��Rx[EBn��H2O��6-n]x++x H+֪��[EBn��H2O��6-n]x+��H+�����ʵ���֮��Ϊ1��x=0.0015mol��0.003mol=1��2����x=2��������Ϊ+3�ۣ��������ܻ��ϼ�Ϊ+2�ۣ��������Ӹ���Ϊ1���仯ѧʽΪ��[CrCl��H2O��5]2+��
�ʴ�Ϊ��[CrCl��H2O��5]2+��
���� ���⿼��λ�ýṹ�������ϵ�����ã�Ϊ��Ƶ���㣬�漰����ﻯѧʽȷ����Ԫ�������ɡ�����ṹ��ԭ�Ӻ�������Ų���֪ʶ�㣬��ȷ���ʽṹ�����ʡ�ԭ�Ӻ�������Ų��ص��֪ʶ���ǽⱾ��ؼ���ע�⣨1���е����Ų��ص㣬Ϊ�״��㣮


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
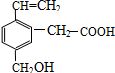 ij�л���ĽṹΪͼ��ʾ�������л�����е������ǣ�������
ij�л���ĽṹΪͼ��ʾ�������л�����е������ǣ�������| A�� | �٢ڢ� | B�� | �٢ڢۢ� | C�� | �ڢۢܢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na | B�� | Mg | C�� | Al | D�� | Zn |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
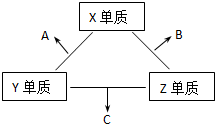 X��Y��Z���ֶ�����Ԫ�أ����ǵ�ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij��������ڳ����¶�����ɫ���壬���ʵ������¿ɷ������±仯��
X��Y��Z���ֶ�����Ԫ�أ����ǵ�ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij��������ڳ����¶�����ɫ���壬���ʵ������¿ɷ������±仯��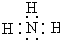 ��C���ӵĽṹ�������Σ�
��C���ӵĽṹ�������Σ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com