
【题目】标准状况下,等质量的O2与O3,一定具有相等的
A. 物质的量 B. 分子数目 C. 体积 D. 原子数目
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是___________。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①___________,③___________。
(3)操作③中所用的有机试剂是CCl4,简述选择其理由_________________________________。
(4)操作过程③可以分解为如下几步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口玻璃塞是否漏液;
D. 倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液;
F. 从分液漏斗上口倒出上层水溶液;
G. 将分液漏斗上口的玻璃塞打开或使玻璃塞上的凹槽或小孔对准分液漏斗口上的小孔;
H. 静置、分层。
a.正确操作步骤的顺序是(填写各操作的编号字母):______→______→_____→A→____→G→E→F。_____
b.上述G步操作的目的是:_________________________________;
c.最后碘的有机溶液是通过___________获得(填“漏斗上口”或“漏斗下口”)。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___________________。
(6)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察下图所示实验装置,指出其所有错误之处__________________________________________。
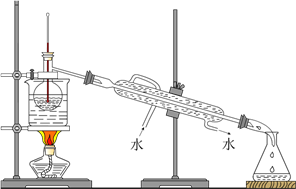
(7)进行上述蒸馏操作时,使用水浴的优点是_______________________________________,最后晶态碘在__________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生取某物质溶于水,制得无色透明溶液,进行以下实验:①与碱反应生成盐和水;②与铁反应生成氢气;③该溶液中阳离子只有H+ . 根据你学过的酸的概念,其中能说明该物质为酸类物质的是( )
A.①②③
B.①②
C.②③
D.③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知食盐常加入KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:
KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
如果反应中转移0.2mol电子,则生成I2的物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.把试剂瓶中的Na2CO3溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂瓶中
B.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
C.将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气
D.用萃取的方法分离汽油和煤油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述中,正确的是( )
A.一定有氧元素参加
B.氧化剂本身发生氧化反应
C.氧化反应一定先于还原反应发生
D.一定有电子转移(得失或偏移)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对化学反应速率与化学反应限度的叙述,不正确的是( )
A.当化学反应达到最大限度时反应速率为0
B.同一化学反应,若反应条件不同,限度可能不同
C.化学反应达到限度时,正逆反应速率相等
D.化学反应的限度与时间的长短无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有由等质量的NaHCO3和KHCO3组成的混合物a g,与100mL盐酸反应。(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示。)
(1)该混合物中NaHCO3与KHCO3的物质的量之比为__________________;
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量为_____________mol;
(3)如果盐酸过量,生成CO2的体积为______________L;
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道_______________;
(5)若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、R、Y、Z、M为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示,R的原子序数大于Z。下列说法错误的是
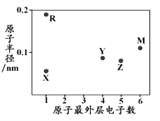
A. R的氧化物只含有离子键
B. 最高价含氧酸的酸性:Y<M
C. 最简单氢化物的稳定性:Y<Z
D. Z的简单氢化物可用作制冷剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com