
��12�֣�
Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�CO2ת����������ȼ���ʡ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪����һ���¡������ܱ������г���l mol CO2��3mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g) ��CH3OH (g)+H2O(g)
 ��H= ��49.0 kJ��mol�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ����ش�
��H= ��49.0 kJ��mol�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ����ش�
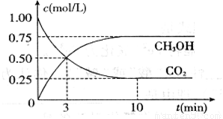
(1)�ﵽƽ���ʱ����____________min(�3����10��)�� ��ǰ10min�ڣ���CO2��ʾ�ķ�Ӧ����
��ǰ10min�ڣ���CO2��ʾ�ķ�Ӧ����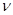 (CO2)=________
(CO2)=________
(2)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� ��
a������ѹǿ���� b�����������c(CO2)����
c��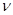 (CH3OH)=
(CH3OH)= 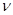 (H2O)
d��c(CH3OH)=c(H2O)
(H2O)
d��c(CH3OH)=c(H2O)
 (3)Ϊ�����H2��ת���ʣ��ɲ�ȡ__________(�����С��)CO2Ũ�ȵĴ�ʩ��
(3)Ϊ�����H2��ת���ʣ��ɲ�ȡ__________(�����С��)CO2Ũ�ȵĴ�ʩ��
(4)��ƽ���H2��ת������_____________��ƽ�ⳣ��K=____________��(����������һλС��)
 �ο�������ϵ�д�
�ο�������ϵ�д� ������ѧ��ʱ��ҵϵ�д�
������ѧ��ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣�Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�CO2ת����������ȼ���ʡ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪����һ���¡������ܱ������г���l mol CO2��3mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g) ��CH3OH (g)+H2O(g) ��H= ��49.0 kJ��mol�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ����ش�
(1)�ﵽƽ���ʱ����____________min(�3����10��)����ǰ10min�ڣ���CO2��ʾ�ķ�Ӧ����![]() (CO2)=________
(CO2)=________
(2)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� ��
a������ѹǿ���� b�����������c(CO2)����
c��![]() (CH3OH)=
(CH3OH)= ![]() (H2O) d��c(CH3OH)=c(H2O)
(H2O) d��c(CH3OH)=c(H2O)
(3)Ϊ�����H2��ת���ʣ��ɲ�ȡ__________(�����С��)CO2Ũ�ȵĴ�ʩ��
(4)��ƽ���H2��ת������_____________��ƽ�ⳣ��K=____________��(����������һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡ�������и߶��ڶ����¿���ѧ�Ծ� ���ͣ������
��12�֣�Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�CO2ת����������ȼ���ʡ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪����һ���¡������ܱ������г���l mol CO2��3mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g) ��CH3OH(g)+H2O(g)


 ��H= ��49.0 kJ��mol�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ����ش�
��H= ��49.0 kJ��mol�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ����ش� ��
��
(1)�ﵽƽ���ʱ����____________min(�3����10��)�� ��ǰ10min�ڣ���CO2��ʾ�ķ�Ӧ����
��ǰ10min�ڣ���CO2��ʾ�ķ�Ӧ���� (CO2)="________"
(CO2)="________"
(2)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�������� �� a������ѹǿ���� b�����������c(CO2)����
a������ѹǿ���� b�����������c(CO2)����
c�� (CH3OH)=
(CH3OH)=  (H2O) d��c(CH3
(H2O) d��c(CH3 OH)=c(H2O)
OH)=c(H2O) (3)Ϊ�����H2��ת���ʣ��ɲ�ȡ__________(�����С��)CO2Ũ�ȵĴ�ʩ��
(3)Ϊ�����H2��ת���ʣ��ɲ�ȡ__________(�����С��)CO2Ũ�ȵĴ�ʩ��
(4)��ƽ���H2��ת������_____________��ƽ�ⳣ��K=____________��(����������һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�������г������߿���ѧ��ģ�Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com