
分析 由①②可知,黄绿色气体B为Cl2,则气体A为HCl,气体B通入石灰水中可以得到漂白粉,是氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,据此分析回答.
解答 解:由①②可知,黄绿色气体B为Cl2,则气体A为HCl,气体B通入石灰水中可以得到漂白粉,是氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,
(1)上述分析可知A为HCl,B为Cl2,
故答案为:HCl,Cl2;
(2)A的浓溶液与MnO2 共热生成氯化锰.氯气和水,反应的化学方程式为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(3)B通入石灰水中制取漂白粉是氯气和氢氧化钙反应生成氯化钙、次氯酸钙和水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
点评 本题考查了物质性质的分析判断,主要是氯气及其化合物性质的理解应用,掌握基础是关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②③④⑥ | B. | ①②⑥ | C. | ②③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅与氢氧化钠溶液 | B. | 氯化氢溶于水 | ||
| C. | 氯化氢与氨反应 | D. | 锌与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
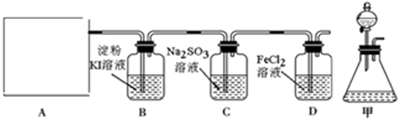
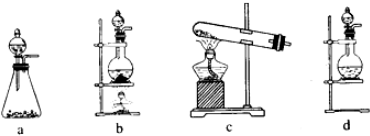
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水的电离方程式:H2O=H++OH- | |
| B. | pH=7的溶液一定是中性溶液 | |
| C. | 升高温度,水的电离程度增大 | |
| D. | 将稀醋酸加水稀释时,c(H+)减小,c(OH-)也减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.| A. | a<b | B. | 上述反应是吸热反应 | ||
| C. | a>b | D. | 上述反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
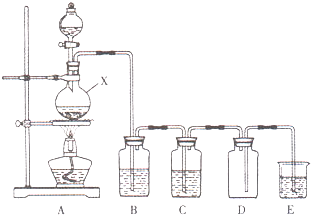 实验室中常用二氧化锰与浓盐酸共热制取氯气.某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如下实验装置.
实验室中常用二氧化锰与浓盐酸共热制取氯气.某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如下实验装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com